Облучение при лечении зубов когда
И другие важные вопросы о «рентгене» в стоматологии
В ходе лечения зубов рентгеновские снимки часто делаются не один раз, а многократно. Пациенты переживают, что это может навредить их здоровью и даже спровоцировать рак. Чтобы развеять их опасения, рассказываем, как работает лучевая диагностика, насколько она безопасна и как часто можно ее проводить.
Как «рентген» видит то, что скрыто?
Основа любого рентгеновского аппарата — катодная трубка, которая испускает рентгеновские лучи (сам первооткрыватель называл их Х-лучами). Лучи проходят сквозь тело пациента и улавливаются расположенным позади него детектором: пленкой, чувствительной к Х-лучам, или цифровой пластиной.
Различные ткани по-разному поглощают рентгеновские лучи. Эти различия позволяют получить на пленке или экране компьютера изображение внутренних органов пациента. Самые плотные структуры (кости) выглядят на снимках белыми, более мягкие (например, мышцы и жир) — серыми, а воздушные полости — черными.
Делать рентген при лечении зубов обязательно?
Зависит от ситуации. Дело в том, что визуально врач может оценить состояние только видимой, наддесневой, части зуба, а остальные его ⅔ скрыты под десной. А еще проблемы могут возникать не только с зубом, но и с окружающими его корень тканями (пародонтом), и костью челюсти. Рентгеновское сканирование помогает узнать, все ли в порядке с этими структурами. По снимкам можно диагностировать, например, периодонтит (воспаление соединительной ткани у корня зуба), абсцессы, кисты или кариес, развившийся под пломбой.
Перед лечением стоматолог делает рентген, чтобы правильно спланировать предстоящие манипуляции. А в процессе и после его завершения — чтобы удостовериться в том, что все было сделано правильно.
Людям со здоровыми зубами и низким риском проблем рекомендуется делать обзорные снимки зубочелюстной системы с профилактической целью каждые 2-3 года. Это позволит вовремя выявлять скрытые патологии, не допуская их перехода в запущенные стадии. После эндодонтического лечения (лечения каналов зуба) проходить рентгеновское обследование желательно ежегодно.
Но ведь радиация — это вредно?
Все зависит от дозы. Выводы о вреде ионизирующего излучения ученые делали, изучая последствия крупных катастроф (в Хиросиме, Нагасаки, Чернобыле). Но в тех событиях люди получали действительно высокие дозы радиации. Достоверных исследований, которые бы доказывали вред малых доз, в частности применяемых в медицине, до сих пор нет.
По всей видимости, лучевая диагностика никак не влияет на наше здоровье. Либо, если и влияет, то не так страшно, как принято думать.
И все же ограничения по лучевой нагрузке есть?
Есть. Согласно российскому законодательству, доза облучения при проведении диагностических рентгеновских процедур не должна превышать 1000 мкЗв (микрозивертов) в год. Причем эта норма касается именно пациентов, и она на самом деле «перестраховочная». Для врачей-рентгенологов, рентгенлаборантов и ряда других профессий допустимые дозы облучения, к примеру, в 20 раз выше — 20 000 мкЗв в год.
Чтобы было понятно, насколько это большие или маленькие цифры, приведем конкретные примеры:
► Доза облучения, которую мы получаем от естественных источников радиации (космических лучей и радона, который выделяется из почвы) составляет порядка 3000 мкЗв в год. Хотя уровень естественного излучения в разных географических районах сильно варьирует. Где-то он может быть и в 200 раз выше средней величины.
► Один трансатлантический перелет дает дозу облучения 80 мкЗв.
► Лучевая нагрузка от маммографии (рентгеновского обследования молочных желез) — 400 мкЗв.
Какая лучевая нагрузка у «рентгена» зубов? Сколько снимков можно делать в процессе лечения?
В стоматологии есть несколько видов рентгеновских исследований, но все они дают небольшую лучевую нагрузку. К примеру, облучение от цифровой радиовизиографии (прицельного снимка зуба) равно 1-3 мкЗв. При проведении цифровой ортопантомографии пациент получает дозу 13-17 мкЗв, при проведении пленочной — 25-30 мкЗв. Компьютерная томография (КТ) зубочелюстной системы дает нагрузку в 45-60 мкЗв.
Исходя из допустимой дозы облучения, в год пациент может делать до 500 радиовизиографических снимков, до 80 цифровых ортопантомограмм и до 20 КТ.
Частоту рентгеновских исследований определяет врач. Если необходимо, за день пациенту может быть сделано несколько рентгеновских процедур. Доза радиации, которую он получит, в любом случае будет небольшой. А в сравнении с рентгеновским исследованием любого другого органа — вообще в десятки раз меньше (просто потому, что другие органы по размеру больше, чем зубы).
А как же рак и лучевая болезнь? Я точно не заболею?
О лучевой болезни можно говорить при дозах радиации свыше 0,7 Зв (это 700 000 мкЗв). А риски онкологических заболеваний достоверно повышаются при дозах свыше 100 000 мкЗв. Даже если сложить дозы радиации от естественных источников и медицинских обследований, цифра все равно получится меньше. Поэтому переживать за здоровье не стоит.
Говорят, красное вино защищает от радиации. Полезно пить его после рентгеновских процедур?
По всей видимости, это миф. Ни в одном руководстве по защите от радиации нет рекомендаций по употреблению красного вина или любого другого алкоголя. Поэтому, что пить, когда и в каких количествах, остается на усмотрение пациентов.
Понравился материал? Ставьте ???? и подписывайтесь. Мы пишем о том, как сохранить здоровье зубов и что делать, если возникли проблемы.
Возможно, вам также будет интересно:
Источник
Лечение зубов у людей, страдающих онкологическим заболеванием, не лишено трудностей. Вместе с тем, избавление от стоматологических недугов необходимо. Ведь больные зубы – источник бактерий.
В арсенале современного стоматолога – множество технологий и методик лечения и протезирование зубов — цены, разновидности и особенности у каждой из них различны. При этом только врач может принять решение, какому лечению отдать предпочтение в каждом конкретном случае. Решение это принимается на основании информации о проблемах и особенностях ротовой полости пациента, а также общем состоянии его здоровья.
Особенно трудным стоматологическое лечение является в случае, если у пациента наблюдается онкологическое заболевание. Вместе с тем, полная санация полости рта у таких больных необходима. Ведь кариес и нездоровые зубы – источник бактерий и вирусов, опасных даже для здорового человека.
Лечение и удаление зубов у онкологических пациентов

Химиотерапия и лучевая терапия зачастую имеют тяжелые побочные эффекты, многие из которых широко известны.
Как правило, они связаны с общим состоянием пациента, например: быстрой утомляемостью, эмоциональной лабильностью, тошнотой, облысением и другими. Однако, кроме общеизвестных осложнений, противораковое лечение нередко также приводит к появлению различных проблем в полости рта.
Лучевая терапия и большинство цитостатических препаратов влияют на активно делящиеся клетки, к которым относятся и клетки слизистой оболочки рта. Под воздействием химиотерапии и облучения происходит торможение их роста, они не успевают обновиться и, как следствие, в полости рта образуется среда, благоприятная для роста патогенных организмов: грибков, бактерий и вирусов.
Это приводит к обострению уже имеющихся проблем:
- кариеса, многократное лечение которого может закончиться удалением зубного нерва;
- гингивита или стоматита;
- пародонтоза;
- увеличению кисты зубов (или ее образованию).
Именно поэтому перед началом прохождения курса химиотерапии или облучения лечение зубов назначается обязательно всем пациентам.
Лучевая терапия и приём некоторых цитостатических препаратов могут привести к осложнениям в полости рта
Повышенной сухости слизистой рта (ксеростомии) как следствие чрезмерного слюноотделения. Это в свою очередь приводит к быстрому накоплению зубного камня и развитию воспаления десен, а также образованию кариозных полостей.
Кровоточивости десен, например, при чистке зубов или употреблении твёрдой пищи (как результат сухости слизистой и снижения тромбоцитов в крови).
Фантомным зубным болям, когда пациент чувствует боль в зубах при отсутствии видимой причины.
Изменению вкуса, нередко пациенты чувствуют странный привкус во рту.
Изъязвлению слизистой полости рта (мукозиту) — это самое опасное осложнение противоракового лечения. В результате облучения или приёма определённых лекарств у онкологических больных обычно сильно снижается уровень нейтрофилов в крови, что значительно повышает риск развития сепсиса — заражения крови. Более того, у таких пациентов этот риск в четыре раза выше, чем у людей с нейтропенией, вызванной другими причинами. Именно поэтому язвы на слизистой рта могут стать причиной прерывания курса терапии.
Химиотерапия и удаление зубов

Казалось бы, когда у человека онкологический диагноз и назначено тяжелое химиотерапевтическое лечение, стоит ли думать о дантисте? Дантисты утверждают, что накануне такого лечения визит к ним обязателен. Незапломбированный зуб, хроническое воспаление десен и другие проблемы во рту во время прохождения химиотерапии могут обернуться обострениями и потерей зубов. А лечить их тогда уже не желательно.
От препаратов, даже мягкого действия, организм ослабляется. Все воспалительные процессы обостряются и труднее лечатся. Например, незапломбированный зуб — это источник инфекций. Не полечили — переходит в воспаление челюсти и может даже доходить до остеомиелита. Челюсть опухает, поднимается температура, появляется боль. Тогда делают разрез челюсти, чтобы вычистить ее от гноя. Нужно принимать антибиотики, а это дополнительная нагрузка на организм. Зуб надо удалять и часто не один. А в сложных случаях иногда приходится удалять даже полчелюсти.
Так что, прежде всего, надо сделать накануне тяжелого химиотерапевтического лечения?
Обязательно нужно запломбировать зубы. Это убережет их от дальнейшего разрушения и во рту не будет источника инфекции, угрозы остеомиелита и потери зубов.
Важно снять зубной камень, потому что он провоцирует воспаление десен. Во время терапии, как известно, иммунитет слабеет и воспаление десен переходит с хронической в острую форму. Даже если ничего не беспокоит до терапии, во время курса могут начаться такие проблемы. Кроме воспаления десен, вследствие зубного камня, также могут расшатываться зубы.
Повторимся: лечить зубы во время терапии не желательно, потому что это дополнительная нагрузка на иммунитет.
Как ухаживать за зубами во время прохождения химиотерапии
В первую очередь, максимально снизить возможность травмирования десен и зубов.
Во-первых, использовать щетку с мягким ворсом. Во-вторых, не употреблять травматическую пищу — рыба с мелкими костями, орехи, сухие и твердые продукты. Даже маленькие травмы могут сильно кровоточить и долго заживать.
Советуют использовать капы. Их изготавливают индивидуально под зубы и челюсти. В середину кладут гель и одевают на зубы на несколько часов. Капы держатся плотно, не спадают. В это время гель работает с зубами. В его составе кальций, фтор, фосфор. Элементы, которых может не хватать зубам при лечении онкологической болезни.
Внимательное отношение больного к состоянию полости рта и высокая квалификация стоматолога сделают лечение зубов не только эффективным, но и абсолютно безопасным для пациента, страдающего онкологическим заболеванием.
Источник
Дмитриева Е.Ф.,
врач-стоматолог, ООО «ТалисманДент М», г. Челябинск
Нуриева Н.С., д.м.н.,
доцент кафедры ортопедической стоматологии ЮУГМУ
Во всем мире рак головы и шеи составляет около 10% всех злокачественных новообразований [1]. Лечение злокачественных новообразований головы и шеи требует мультидисциплинарного подхода, сотрудничества врачей различных специальностей: хирурга-онколога, радиолога, химиотерапевта, рентгенолога, эндоскописта, стоматолога, патоморфолога, цитолога, а также врачей некоторых других специальностей, каждый из которых участвует в установлении диагноза, оценки степени распространения опухоли, выработке тактики лечения и его проведении [2]. Выбор стратегии и лечения в основном осуществляется между хирургическим лечением, лучевой терапией и комбинированными методами.
Лучевая терапия – метод лечения с использованием ионизирующего излучения. Среди различных методов лечения в клинической онкологии лучевая терапия занимает одно из ведущих мест. По данным ВОЗ, 70-75% онкологических больных нуждаются в проведении лучевой терапии. Облучение может быть радикальным, паллиативным или используется в комбинации с операцией. К преимуществам лучевой терапии следует отнести ее хорошую переносимость, возможность достижения в ранних стадиях некоторых опухолей стойкого излечения с сохранением функции пораженного органа. Применение лучевого лечения в качестве паллиативной, самостоятельной терапии в неоперабельных случаях является самым эффективным среди других лечебных мероприятий.
В лучевой терапии органов головы и шеи в самостоятельном плане для получения радикального или паллиативного эффекта широко применяется подобранный ритм ежедневного облучения по 2 г (5 раз в неделю; за неделю – 10 г). Суммарная очаговая доза при этом составляет (при средней радиочувствительности опухоли) 60-70 г. Лучевая терапия проводится по расщепленной программе: первый курс – до суммарной очаговой дозы 30 г, затем следует перерыв в лечении на 2-3 нед. Второй курс проводится также разовой очаговой дозой 2 г до суммарной очаговой дозы 40 г (общая суммарная доза – 70 г) [3].
Однако проблемой при этом остается довольно высокая частота тяжелых посттерапевтических осложнений, существенно снижающих возможности метода лечения. Частым осложнением лучевой терапии является лучевое поражение зубов (рис. 1).
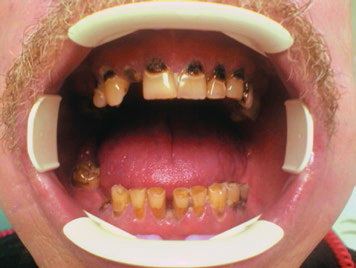
Рис.1. Лучевой некроз зубов после курса лучевой терапии (54 г)
Одним из перспективных направлений в этом плане является использование современных технических достижений, позволяющих снизить объем нежелательно облучаемых нормальных тканей с концентрацией максимальной дозы излучения на уровне опухоли и на этой основе улучшить результаты лечения этого контингента больных [4].
С целью повышения эффективности лучевой терапии обосновано применение режимов гиперфракционированного облучения. По мнению некоторых отечественных и зарубежных исследователей, увеличение разовой очаговой дозы до 2,4-3 г при условии подведения последней за 2-3 фракции в сутки с интервалом между фракциями не менее 4 часов сопровождается повышением эффективности лечения рака носоглотки на 20-30% [5,6]. В исследовании, выполненным S.L. Wolden и соавт., которые провели сравнительный анализ результатов облучения в обычном режиме фракционирования дозы (1,8 г/5 раз в неделю/70 г) и динамического фракционирования, когда в течение 5-й и 6-й недель проводится облучение с использованием ускоренного фракционирования разовой дозой 1,6 г 2 раза в день в сочетании с химиотерапией цисплатином. Отмечено статистически значимое увеличение частоты полной резорбции опухоли, безрецидивной и общей выживаемости [14]. По результатам исследований ряда авторов, ранние лучевые повреждения со стороны слизистой оболочки встречались значительно чаще при гиперфракционировании. Однако число поздних лучевых повреждений было одинаковым [7].
Не меньшее значение уделяется качеству проведения лучевой терапии. Применение особых приспособлений (подголовники, маски из термоплавких пластмасс), фиксирующих определенное положение больного в процессе облучения, индивидуальное дозиметрическое планирование на основе рентгеновской компьютерной томографии и формирование динамически изменяющихся фигурных полей облучения с помощью мультилифтного коллиматора способствуют повышению эффективности лучевой терапии. В сравнении со стандартной программой лучевой терапии применение методики конформного облучения на основе трехплоскостного планирования позволяет создать оптимальное соотношение между дозой излучения, подводимой к опухоли и в окружающих тканях [8].
Лучевые поражения твердых тканей зуба при длительном воздействии на организм малыми дозами зависят от суммарной дозы, облучения, интенсивности облучения и фактора времени. Изменения в тканях зуба проявляются в виде меловых пятен, пигментации, размягчения и некроза эмали и дентина (рис. 2).
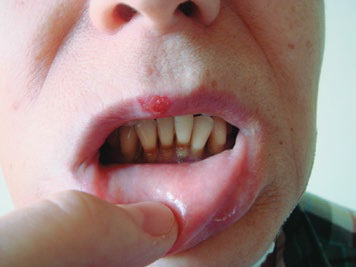
Рис.2. Лучевой кариес после сплит-курса лучевой терапии
Большие дозы облучения могут приводить к некрозу больших участков эмали и дентина в области иммунных зон зубов. Изменения в пульпе проявляются в виде гиалинизации стенок сосудов, вакуольного и жирового перерождения, атрофии и дегенерации одонтобластов и т.д. Комплекс патоморфологических изменений в тканях зуба при этих поражениях во многом напоминает кариес зубов, что дало основание ввести термин лучевой кариес.
Лучевой кариес зуба – (c. dentis radialis) генерализованный кариес зуба, развивающийся как осложнение рентгено- или радиотерапии челюстно-лицевой области; протекает с пигментацией и размягчением поверхностных слоев и образованием глубоких пришеечных полостей.
До настоящего времени не разработано единое мнение по поводу механизма и характера изменений в тканях зуба и полости рта вследствие радиационного излучения.
Иванова Л.А. считает, что возникающие под влиянием ионизирующего излучения распад белковых молекул, нарушения обменных процессов, расстройства кровообращения, гипоксия в совокупности способствуют развитию неблагоприятных условий существования пульпы, и чем дольше они будут иметь место, тем более тяжелыми могут быть последствия как для пульпы, так и для твердых тканей зуба [9]. По мнению Барер Г.М., Иванчиковой Л.А., в основе изменений твердых тканей лежат повреждения белковой матрицы и нарушение химической связи между минеральной и белковой фракциями. Уже в процессе облучения авторы наблюдали в дентине и цементе зубов экспериментальных животных деминерализацию и деструктивные изменения, что можно объяснить особенностями гистологического строения твердых тканей, чрезвычайно низким обменом веществ в них, неспособностью тканей к восстановлению [10].
По данным Окадо Ш., 1979, дальнейшее развитие возникших во время облучения изменений дентина, характеризующиеся продолжающейся деминерализацией, увеличением очагов деструкции, разрушением эмалево-дентинного соединения, появлением лакунарного рассасывания дентина на границе с пульпой объясняется как реакцией последствия, так и влиянием поврежденной пульпы, восстановление которой после облучения является неполным. В разрушении эмалево-дентинного соединения имеет значение различие в интенсивности деминерализации эмали и дентина. Насыщенность минеральными веществами дентина снижается в значительно большей степени, чем эмали, что приводит к дезинтеграции этих тканей.
Иванова Л.А., Боровский Е.В., Сегень И.Т. и Назаров Г.И. указывают, что патологический процесс возникает одновременно во многих зубах, распространяется вокруг шеек и по поверхностям коронок, заканчиваясь, как правило, отломом зуба на уровне десневого края. Авторами обращается внимание на неэффективность пломбирования из-за появления вокруг пломб, а также в ранее неповрежденных участках новых дефектов [9, 11, 12].
Изменения на слизистой оболочке полости рта, на что указывает Щелканогова М.Г. и соавт., 1993, плохая гигиена в комплексе приводят к нарушению самоочищения зубов, на поверхности эмали создается критическая ситуация (pH 4-5 под налетом), благоприятствующая деминерализации облученной эмали. Повышается чувствительность зубов к изменениям температуры, к давлению, к сладкому и кислому, изменяется цвет (до светло- или темно-серого), эмаль теряет блеск, становится ломкой хрупкой; зубы покрыты толстым клейким трудноудаляемым налетом. Появляется кариесогенная микрофлора. Кариес возникает и на сравнительно редко поражаемых участках (в области бугров, на режущих отделах). Наиболее характерен пришеечный кариес передних зубов. Процесс протекает безболезненно, быстро прогрессирует и заканчивается отломом коронок.
Принципы профилактики и лечения отражены в протоколе Dental Disease Section/International Society of Oral Oncology (ISOO) (2010):
1. Применение фторидсодержащих препаратов. Реминерализующая терапия значительно снижает риск развития патологии твердых тканей зубов (Level of Evidence: II, Grade of Recommendation: B), (рис. 3).
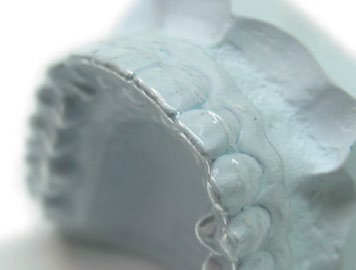
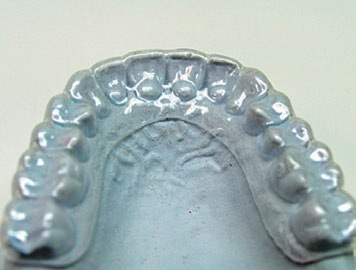
Рис.3. Каппы для реминерализующей терапии
2. Применение полосканий для полости рта с хлоргексидином. Использование этих препаратов улучшает гигиеническое состояние полости рта, а также способствует снижению числа Streptococcus mutans. При назначении хлоргексидин содержащих полосканий необходимо принимать к сведению возможность возникновения таких побочных эффектов как окрашивание зубного камня и изменение вкусовой чувствительности (Level of Evidence: II, Grade of Recommendation: B).
3. Восстановление дефектов твердых тканей зубов. Для восстановления дефектов твердых тканей зубов рекомендуется использовать композитные материалы, гибридные стеклоиономерные цементы и амальгаму. Применение традиционных СИЦ менее предпочтительно (Level of Evidence: II, Grade of Recommendation: B) [13].
При поражении твердых тканей коронки зуба лечение проводят в несколько этапов. Вначале осторожно удаляют некротические массы из дефектов зубов вручную экскаватором, чтобы не внедриться в полость зуба, а затем вводят кальцифицирующую пасту, состоящую из равных частей порошка глицерофосфата кальция, оксида цинка и глицерина. Пасту накладывают тонким слоем на дно и стенки образовавшейся полости и закрывают временным пломбировочным материалом.
Следующий этап отсроченного лечения зубов проводят через 1-1,5 мес. Он состоит в удалении нежизнеспособных, некротизированных тканей зуба при помощи бора до минерализованного участка дентина или эмали, после чего вновь накладывают кальцифицирующую пасту и пломбируют зубы стеклоиономерными цементами.
При более глубоких поражениях устраняют имеющиеся некротические дефекты стеклоиономерными цементами и через 3-4 месяца, если этого требует косметическая реставрация передних зубов, часть стеклоиономера удаляют, а сверху накладывают композитный пломбировочный материал.
Таким образом, лучевой кариес является распространенным осложнением лучевой терапии рака орофарингеальной зоны. На сегодняшний день разнятся мнения о клинической картине, особенностях течения заболевания и тактике лечения. Нами не найдены данные в литературе о зависимости режимов фракционирования и лучевыми повреждениями зубов в ранние и отдаленные сроки, а также о влиянии конформного облучения на твердые ткани зуба. Планируем более детальное изучение проблемы.
Список литературы:
1. Черенков В.Г. Клиническая онкология: учеб. пособие для системы постдиплом. образования врачей / В.Г. Черенков. – Изд. 3-е, испр. и доп. – М.: МК, 2010. – 434 с.
2. Кропотов М.А. Общие принципы лечения больных первичным раком головы и шеи / М.А. Кропотов // Практическая онкология. – 2003. – Т.4, №1. – С.1-7.
3. Онкология: учебник для вузов / Вельшер Л.З., Матякин Е.Г., Дудицкая Т.К., Поляков Б.И. – 2009. – 512 с.
4. Алиева С.Б. Химиолучевая терапия больных с местнораспространенным плоскоклеточным раком головы и шеи/ С.Б.Алиева // Практическая онкология. – 2008. – Т.9, №1. – С.27-30.
5. Алиев Б.М., Гарин А.М., Кошалиев Э.Ш. Сравнительная оценка эффективности лучевого и химиолучевого лечения местнораспространенного рака носоглотки III-IV стадиями заболевания // Мед. радиол. – 1987. – №7. – С. 25-30.
6. Алиев Б.М., Гарин А.М., Чуприк-Малиновская Т.П. Рак носоглотки: опыт лучевого и химиолучевого лечения // Вестн. ОНЦ РАМН. – 1995. – №1. – С. 26-32.
7. Канаев С.В. Лучевая терапия злокачественных опухолей головы и шеи/ С.В.Канаев // Практическая онкология. – 2003. – Т.4, №1. – С. 15-24.
8. Чуприк-Малиновская Т.П. Рак носоглотки: вопросы диагностики и лечения // Практическая онкология. – 2003. – Т.4, №1. – С. 38-44.
9. Иванова Л.А. Профилактика постлучевых поражений зубов.//Методические рекомендации. – Пермь, 1987.
10. Барер Г.M. Изменения ультраструктуры твердых тканей зубов после местного облучения // Г. М. Барер, Л. А. Иванчикова; Г. И. Назаров // Стоматология. 1977. – №1. – С. 4-7.
11. Боровский Е.В., Сазонов Н.И. Изменение проницаемости эмали зубов после дистанционного гамма-облучения нижней челюсти // Стоматология. – 1978. – С.1-5.
12. Назаров Г.И. Изменение зубов и челюстей после локального гамма-облучения // Мед. радиология. – 1975. – №8. – С.75-76.
13. Боровский Е.В. Реставрация лучевого кариеса зубов. Клинический пример/Е.В. Боровский, И.М. Макеева, Е.А. Скатова// Стоматология детского возраста и профилактика: рецензируемый, рекомендованный ВАК научный журнал. – 2012. – Т. XI, №2. – С.11-19.
14. Wolden S.L., Zelefsky M.J., Kraus D.H. et al. Accelerated concomitant boost radiotherapy and chemotherapy for advanced nasopharyngeal carcinoma // J. Clin. Oncol. – 2001/ – Vol. 19(4). – P. 1105-1110.
Статья предоставлена журналом «Проблемы стоматологии»
Источник

