Паклитаксел в лечении рака молочной железы
Паклитаксел относится к группе таксанов и является относительно хорошо изученным цитостатиком, поскольку опыт его клинического применения приближается к 15 годам. Этот срок позволяет сравнительно четко и объективно обозначить ту нишу, которую препарат занимает в лечении различных опухолей.

Таблица 1. Эффективность некоторых режимов химиотерапии в сочетании и без трастузумаба
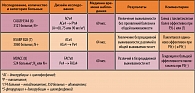
Таблица 2. Итоги исследований по адъювантной терапии рака молочной железы с участием паклитаксела

Таблица 3. Эффективность режимов с включением паклитаксела в неоадъювантной химиотерапии рака молочной железы.
Паклитаксел является одним из основных препаратов в терапии целого ряда злокачественных новообразований, в частности рака молочной железы, яичников, легких, эпителиальных опухолей головы и шеи, т.е. наиболее часто встречающихся нозологических форм.
Рак молочной железы – одна из первых локализаций, при которой паклитаксел проявил выраженную противоопухолевую активность сначала в монотерапии у многократно леченных ранее больных, в том числе резистентных к антрациклинам, а затем в первой линии химиотерапии, а также в комбинациях с другими цитостатиками. Как и следовало ожидать, наиболее эффективными оказались режимы с включением паклитаксела и антрациклинов, однако при высокой непосредственной эффективности в большинстве исследований не удалось существенно улучшить отдаленные результаты лечения. В связи с этим целесообразность использования подобных комбинаций в первой линии химиотерапии по-прежнему остается спорным вопросом. Очевидно, в первую очередь такие режимы должны назначаться больным с массивным опухолевым процессом и быстрым темпом прогрессирования болезни.
Итоги многочисленных работ, посвященных использованию паклитаксела в различных клинических ситуациях, подробно освещены в литературе предыдущих лет (1), поэтому в нашей статье мы сделаем акцент на новых аспектах использования препарата, а также подведем итоги некоторых крупных сравнительных исследований, результаты которых стали доступны в последнее время.
Следует отметить, что комбинации паклитаксела с другими цитостатиками относительно хорошо охарактеризованы, хотя исследования в этом направлении продолжаются. Перспективы же дальнейших исследований с участием паклитаксела видятся в изучении его комбинаций с таргетными препаратами и, соответственно, поиске оптимальных сочетаний такого рода, а также в осмыслении роли паклитаксела как одного из представителей группы таксанов в лечении раннего рака молочной железы.
Что касается комбинаций с таргетными препаратами, то сегодня сравнительно хорошо изученными являются комбинации паклитаксела с трастузумабом, единственным пока препаратом этой группы, разрешенным к клиническому применению при раке молочной железы в России. Еще на этапе доклинического изучения было отмечено аддитивное взаимодействие паклитаксела и трастузумаба (2). В дальнейшем эти факты нашли подтверждение в соответствующих клинических исследованиях. Наиболее показательными являются данные рандомизированного исследования H0648g, в котором приняли участие 469 больных метастатическим раком молочной железы с гиперэкспрессией Her-2/neu (3). Все больные были рандомизированы на две группы: в первой проводилась стандартная химиотерапия (паклитаксел 175 мг/м2 1 раз в 3 нед. для больных, получавших антрациклины адъювантно, или стандартные режимы АС/ЕС для больных, не получавших ранее химиотерапии); во второй группе эти же режимы химиотерапии назначались в сочетании с трастузумабом в стандартной дозе 2 мг/кг еженедельно. Оказалось, что комбинация паклитаксела с трастузумабом обладает большей эффективностью как в отношении непосредственных, так и отдаленных результатов (таблица 1).
Комментируя это исследование, следует отметить, что антрациклинсодержащие комбинации были также более эффективными в комбинации с трастузумабом, однако, такого рода режимы не рекомендованы сегодня для использования в повседневной клинической практике по причине суммирования кардиотоксических эффектов, свойственных как трастузумабу, так и антрациклинам.
Высокоэффективными оказались еженедельные схемы введения паклитаксела в дозе 90 мг/м2 и трастузумаба в стандартной дозе. При продолжительности лечения 25 недель объективные противоопухолевые эффекты были получены у 67-81% больных с гиперэкспрессией Her-2/neu в зависимости от метода определения уровня экспрессии. В противоположность этому эффективность такого режима лечения у больных с нормальным уровнем экспрессии Her-2/neu составила всего 41-46% (4).
Чрезвычайно интересными представляются данные рандомизированного исследования III фазы Е2100, в котором проведено сравнение эффективности и токсичности монотерапии паклитакселом (90 мг/м2 1, 8 и 15 дни 1 раз в 4 нед.) с комбинацией паклитаксела и бевацизумаба (10 мг/кг 1 и 15 дни 1 раз в 4 нед.) в первой линии лечения. В исследовании приняли участие 722 больных распространенным раком молочной железы. Комбинированный режим позволил существенно улучшить показатели непосредственной эффективности (частота объективных эффектов 28,2% vs. 14,2%; р
Таким образом, комбинированное применение паклитаксела с таргетными препаратами существенно расширяет возможности химиотерапии рака молочной железы.
Важное направление в изучении таксанов вообще и паклитаксела в частности связано с оценкой роли этих препаратов в лечении раннего рака молочной железы. Этот вопрос в настоящее время продолжает интенсивно изучаться. Достаточно сказать, что сегодня в литературе имеются сообщения как минимум о 19 исследованиях, посвященных раннему раку молочной железы, где в адъювантных режимах используются таксаны; общее количество участниц в этих исследованиях составляет 35500. Результаты 8 исследований имеют достаточный для анализа срок наблюдения. Остановимся подробнее на работах, в которых в режимах адъювантной терапии был использован паклитаксел (таблица 2).
В исследовании CALGB 9344, одном из наиболее влиятельных в истории медицинской онкологии, приняли участие 3121 больных с положительными подмышечными лимфоузлами. Целью работы было выяснить, повлияет ли увеличение дозы доксорубицина или добавление паклитаксела к стандартному режиму АС на отдаленные результаты лечения. При медиане времени наблюдения 69 мес. выявлено статистически значимое снижение риска рецидива (на 17%) и смерти (на 18%) в группе больных, получавших паклитаксел. При анализе результатов лечения в различных подгруппах больных существенное увеличение безрецидивной выживаемости отмечено только у пациенток с РЭ (-) опухолями. Доза доксорубицина не оказала существенного влияния на результаты лечения (6).
Проект NSABP B-28 с участием 3060 больных с метастазами в подмышечные лимфоузлы предполагал сравнение в качестве адъювантной терапии 4 курсов АС и сочетания 4 курсов АС с последующими 4 курсами паклитаксела. При медиане времени наблюдения 64 мес. в группе больных, получавших паклитаксел, выявлено статистически значимое снижение риска рецидива; существенного влияния на общую выживаемость не отмечено. Паклитаксел был одинаково эффективным независимо от рецепторного статуса опухоли (7).
В небольшом исследовании MD Andersen приняли участие 524 больных, которые получали либо 4 курса паклитаксела с последующими 4 курсами FAC, либо 8 курсов FAC. При медиане времени наблюдения 60 мес. статистически значимых различий в общей и безрецидивной выживаемости выявлено не было, хотя имелась тенденция к улучшению этих показателей в группе паклитаксела (8).
Данные исследований по адъювантной терапии с включением таксанов были проанализированы экспертами и отражены в очередном консенсусе по лечению раннего рака молочной железы, принятом в Сан Галлене в 2005 г. (9). Было отмечено, что имеющиеся данные пока не позволяют рекомендовать таксаны в качестве адъювантной терапии у больных с N(-). Что касается больных с N(+), то экспертами отмечено несовершенство дизайна ряда исследований, в частности обусловленное включением больных с различным рецепторным статусом, что могло исказить истинную картину эффективности химиотерапии. Поэтому значение таксанов, и в частности паклитаксела в адъювантной терапии рака молочной железы, по-прежнему требует уточнения. Между тем, выбор в пользу дополнения антрациклиновых режимов таксанами, в т.ч. паклитакселом, может быть сделан, во-первых, в подгруппе больных с повышенным риском рецидива (высокая экспрессия Her-2/neu, отрицательный рецепторный статус), а во-вторых, в тех клинических ситуациях, когда мы по каким-то причинам предполагаем наличие повышенного риска развития кардиотоксичности.
Высокая противоопухолевая активность паклитаксела, особенно в сочетании с антрациклинами, у больных диссеминированным раком молочной железы сделала обоснованной попытку применения его в режимах неоадъювантной химиотерапии. Как известно, при проведении такого варианта лечения в наибольшей степени выигрывают те больные, у которых в результате химиотерапии достигнута полная морфологическая регрессия опухоли. Возможности паклитаксела в неоадъювантной химиотерапии раннего рака молочной железы были оценены в соответствующих клинических исследованиях (таблица 3).
Впечатляющие результаты были получены группой итальянских ученых, использовавших у больных с T2-3N0-1 в качестве неоадъювантной химиотерапии комбинацию цисплатина 30 мг/м2, эпирубицина 50 мг/м2 и паклитаксела 120 мг/м2 еженедельно в течение 8 недель с поддержкой колониестимулирующими факторами. Объективные противоопухолевые эффекты были получены у 98% больных, в том числе у 50% – полные, при этом у 35% больных полная морфологическая регрессия опухоли была достигнута не только в молочной железе, но и в подмышечных лимфоузлах (!) (17).
Поистине сенсационными являются первые данные, полученные в небольшом исследовании с участием 42 больных с T1-4N0-2 и гиперэкспрессией Her-2/neu при использовании последовательно 4 курсов FEC и 4 курсов паклитаксела в сочетании с трастузумабом: сообщается о 66,7% полных морфологических регрессий (!) (18).
Результаты применения паклитаксела в неоадъювантной химиотерапии, безусловно, выразительны, но требуют дальнейшего подтверждения при долгосрочном наблюдении за больными. Однако подобные комбинации уже сейчас могут применяться на дооперационном этапе, особенно у больных с большими опухолями, а также другими факторами повышенного риска.
Стремление улучшить результаты лечения раннего рака молочной железы заставляет продолжать поиск новых эффективных стратегий и в адъювантной терапии, особенно в группе больных с неблагоприятным прогнозом. Эффективность адъювантной химиотерапии с включением наиболее эффективных препаратов (антрациклинов, паклитаксела, трастузумаба) интенсивно изучается сегодня в соответствующих рандомизированных исследованиях. Предварительные данные двух из них — NCCTG №9831, NSABP B-31 – уже опубликованы.
Дизайн этих исследований был схожим и предполагал проведение 4 курсов химиотерапии по схеме АС, после которых проводились 4 курса паклитаксела в сочетании или без трастузумаба, который назначался на срок
1 год. Абсолютный выигрыш при использовании трехкомпонентного варианта лечения (АС + паклитаксел + трастузумаб) в течение 3 и 4 лет составил соответственно для безрецидивной выживаемости 12% и 18%, для отдаленного метастазирования – 9% и 16%, для общей выживаемости – 2,5% и 4,8%. Следует отметить, что 19% больных прекратили лечение трастузумабом в связи с кардиотоксичностью (19).
Кроме того, протоколом исследования NSABP B-31 было предусмотрено сравнение одновременного и последовательного c паклитакселом назначения трастузумаба. Оказалось, что одновременное с паклитакселом назначение трастузумаба улучшило безрецидивную выживаемость на 36% (р=0,014) по сравнению с последовательным (20).
Таким образом, паклитаксел является сегодня неотъемлемой составной частью лечебных программ при диссеминированном и раннем раке молочной железы, ощутимо влияя на эффективность терапии. Интенсивное развитие фармакотерапии рака молочной железы и появление принципиально новых классов противоопухолевых средств открывает дополнительные перспективы использования препарата, требующие его изучения в новых условиях применения. Основной тенденцией современности в лечении опухолей и в частности рака молочной железы является индивидуальный подбор лечебной тактики, основывающийся на детальной характеристике опухоли на генном уровне. Такой подход, возможно, позволит более четко обозначить круг больных, которым показано назначение таксанов, в том числе паклитаксела, что должно сделать терапию более эффективной.
Источник
Спонсор исследования: Vanderbilt-Ingram Cancer Center (Теннеси, США), соавтор: Национальный институт рака (NCI). Дата проведения: 2011—2017 гг.
Эверолимус — таргетный препарат, который ингибирует протеинкиназы, тем самым блокируя размножение раковых клеток и приток крови к опухолевой ткани. Цисплатин и паклитаксел — химиопрепараты с разными механизмами действия. Ученые предположили, что комбинированная терапия тремя данными препаратами могла бы более эффективно уничтожать опухолевые клетки. Целью исследования стала проверка эффективности цисплатина, паклитаксела и Эверолимуса при метастатическом раке молочной железы.
В первой фазе исследования был оценен профиль безопасности препаратов. Во второй фазе — выживаемость без прогрессирования.
В исследовании приняли участи 55 пациентов: 54 женщины и один мужчина с метастатическим раком молочной железы. 47 участников (85,5%) находились в возрасте 18–65 лет, 8 (14,5%) были старше 65 лет.
Лечение проводилось по следующей схеме:
- Эверолимус перорально один раз в день ежедневно.
- Цисплатин внутривенно один раз в неделю в течение трех недель, затем недельный перерыв.
- Паклитаксел внутривенно один раз в неделю в течение трех недель, затем недельный перерыв.
Таким образом, продолжительность цикла составила 4 недели. Всем участникам были назначены одинаковые начальные дозировки препаратов.
Максимальные переносимые дозы (МПД) были оценены как дозы, предшествовавшие тем, что вызывали дозозависимую токсичность у 2 из 3 пациентов. Для цисплатина это значение составило 25 мг/м2, для паклитаксела — 80 мг/м2, для Эверолимуса — 5 мг.
Выживаемость без прогрессирования оценивалась по количеству пациентов, которые остались в живых спустя 6 месяцев с начала лечения, и у которых за это время не отмечалось признаков прогрессирования заболевания. Данный показатель удалось проанализировать у 51 пациента (четверо в течение первых 6 месяцев прекратили участие в исследовании из-за побочных эффектов препарата). Прогрессирования не отмечалось у 21 пациента (41%).
Среди наиболее частых побочных эффектов у участников исследования были отмечены: нарушения со стороны крови (нейтропения, анемия, тромбоцитопения), боли в животе, одышка, лихорадка, тошнота и рвота, боли в мышцах и костях.
Полный ответ на терапию был получен у одного пациента (исчезновение очагов), частичный ответ — у 12 пациентов (уменьшение максимального диаметра очага на 30%). В 27 случаях удалось добиться стабилизации опухолей (отсутствие значимого увеличения или уменьшения диаметра очага), в 11 — болезнь продолжила прогрессировать (увеличение максимального диаметра на 20%).
Лечение рака с метастазами — сложная задача. Как правило, оно носит паллиативный характер и направлено на увеличение продолжительности жизни пациента. Важно правильно подобрать комбинации препаратов, которые будут наиболее эффективно уничтожать раковые клетки, но при этом вызывать минимум побочных эффектов. В этом помогают молекулярно-генетические исследования. В Европейской клинике можно составить «молекулярный портрет» опухоли и назначить персонализированную терапию. Мы знаем, как повысить эффективность химиотерапии, что делать, если химиопрепараты перестали работать. Свяжитесь с нами.
Запись
на консультацию
круглосуточно
Источник: https://clinicaltrials.gov/ct2/show/NCT01031446?term=cancer&recrs=e&rslt=With&type=Intr&rank=6
Источник
Одним из самых популярных противоопухолевых препаратов на сегодняшний день является “Паклитаксел”. Это лекарственное средство растительного происхождение, которое выделяют из коры тисового дерева. Также, его получают путем синтеза и полусинтеза.
Клинические исследования и противораковые свойства
“Паклитаксел” обладает цитотоксическим антимикотическим эффектом. Он относится к таксанам, которые начали применяться для лечения онкологических заболеваний в 90-х годах ХХ столетия. Введение в схему терапии “Паклитаксела” при раке яичника, позволило увеличить эффективность такой терапии до 79%, а количество полных регрессий достигло 46%.
“Паклитаксел” является первым препаратом, который продемонстрировал высокую эффективность (от 16% до 50%) при лечении пациенток, страдающих злокачественными новообразованиями яичников, у которых до этого терапия медикаментами платины была неэффективной.
В США его широко начали использовать при раке яичника с 1992 года, а в 1998 году он был одобрен FDA в качестве лечения первой линии при этом заболевании. Его комбинация с “Карбоплатином” стала стандартной схемой терапии.
“Паклитаксел” стали широко внедрять в повседневную клиническую практику. Его назначали в комплексе с “Цисплатином” или “Карбоплатином”. Но в 1995—1998 гг., было произведено исследование, которое показало, что отдельное применения “Карбоплатина” по эффективности не уступает при его совместном назначении с “Паклитакселом”, а если учитывать какое количество нежелательных реакций возникает на фоне такой комбинации, то монотерапия “Карбоплатином” при раке яичника I—III стадии оказалась предпочтительней.
Преимущество схем лечения, в который входил “Паклитаксел”, было очевидным только у пациенток с остаточной опухолью больше 1 см.
В ходе клинических исследований, было выявлено усиление терапевтического эффекта при одновременном применении “Паклитаксела” со следующими препаратами:
- “Гемцитабин”;
- “Топотекан”;
- “Фторурацил”;
- “Цисплатин”;
- “Циклофосфамид”;
- “Этопозид”;
- “Винкристин”.
В ходе проведенных клинических исследований, “Паклитаксел” доказал свою высокую эффективность, особенно при лечении пациентов с неблагоприятным прогнозом, когда остаточный размер новообразования более 1 см.
После внутривенного введения лекарственное средство связывается с белками плазмы, время полураспределения из кровотока в ткани составляет полчаса. Быстро проникает и всасывается тканями, депонируется во многих внутренних органах. Проходя печень, подвергается метаболизму, при повторном введении не кумулирует. Выводится через почки.
При каких видах рака показан “Паклитаксел”?
Препарат прописывают пациентам страдающим:
- раком яичника;
- раком груди;
- немелкоклеточным раком легкого;
- саркомой Капоши.
Состав и действующее вещество
Лекарственное средство выпускается в виде концентрата для изготовления инфузионного раствора, который в качестве действующего вещества содержит 6 мг паклитаксела. В качестве дополнительных компонентов препарат содержит:
- безводный этиловый спирт;
- азот;
- кремофор EL.
Дозировка и правила введения
Схема лечения подбирается в индивидуальном порядке. Каждому пациенту, чтобы предупредит тяжелые реакции гиперчувствительности, перед началом терапии проводят премедикацию. Для этой цели вводят следующие препараты:
- “Дексаметазон” в таблетках в дозировке 20 мг (при саркоме Капоши в дозировке от 8 до 20 мг) за 12 ч. и 6 ч. до вливания “Паклитаксела” или инъекций за 0,5—1 ч. до введения противоопухолевого средства.
- “Дифенгидрамин” в дозировке 300 мг, “Хлорфенирамин” 10 мг, “Ранитидин” 50 мг, “Циметидин” 300 мг в виде внутривенных инъекций за 30 – 60 минут до инфузий “Паклитаксела”.
Лекарственное средство при раке яичников вводят в виде внутривенных инфузий в следующих дозировках:
- В качестве химиотерапии первой линии: в дозировке 175 мг/м2 на протяжении 3 ч., после этого через каждый 21 день вводят “Цисплатин” или же в дозировке 135 мг/ м2 в течение суток после чего также каждые 3 недели назначают “Цисплатин” (в таких же дозировках “Паклитаксел” прописывают при немелкоклеточном раке легкого).
- В качестве терапии второй линии: в дозировке 175 мг/м2 каждые 3 недели.
“Паклитаксел” при раке груди прописывают в дозировке 175 мг/м2 в течение 3 ч. 1 раз в 3 недели:
- Адъювантную терапию проводят после завершения стандартного комплексного лечения, всего делают 4 вливания медикамента.
- Терапию первой линии назначают после завершения адъювантного лечения.
- Терапию второй линии проводят у пациентов, у которых перенесенная химиотерапия была неудачной.
При ангиосаркоме у больных СПИДом “Паклитаксел” рекомендуется прописывать как терапию второй линии, после неудачной химиотерапии. Его назначают в дозе 135 мг/м2 через каждые 21 день или в дозировке 100 мг/ м2, каждые 14 дней. Вводят медикамент в виде 3-х часовых инфузии.
В зависимости от тяжести иммунодепрессии у больных СПИДом, лечение рекомендуется назначать только когда количество нейтрофилов будет минимум 1000/мкл, тромбоцитов — 75000/мкл.
Если у пациента наблюдается снижение количества тромбоцитов, ниже 500/мкл на протяжении недели или выраженная форма нейтропении, мукозита то дозировку нужно снижать на 25%, пока она не составит 75 мг/м2.
Пациентам, страдающим нарушениями функции печени, дозировка подбирается в зависимости от активности ее энзимов и уровня билирубина в крови.
Перед тем, как ввести препарат, концентрат нужно развести в физрастворе, растворе 5% глюкозе, раствором 5% декстрозы в физрастворе или растворе Рингера, чтобы получилась концентрация 0,3—1,2 мг в 1 мл. Полученный раствор может опалесцировать.
Готовить раствор должен специально обученный персонал с соблюдением условий асептики. При этом руки должны быть защищены перчатками. Нужно избегать контакта лекарства с кожей и слизистыми, но если это произошло, медикамент надо смыть водой.

Механизм действия
“Паклитаксел” нарушает процесс деления клеток. Он стимулирует сборку микротрубочек из димерного белка тубулина, подавляет их деполимеризацию, в результате они стабилизируются, блокируется их динамическая реорганизация в интерфазе и во время митоза. Индуцирует патологическое скопление микротрубочек в виде пучков весь клеточный цикл и одновременно способствует образованию множественных звезд микротрубочек при делении клетки.
Противопоказания и важные ограничения к применению
Лекарственное средство противопоказано, если наблюдается:
- индивидуальная непереносимость состава препарата;
- тяжелые патологии печени;
- период вынашивания ребенка;
- лактация;
- возраст младше 18 лет;
- исходное количество нейтрофилом меньше 1,5 ·10 9/л у больных с большими размерами новообразования;
- тяжелые неконтролируемые инфекционные заболевания у пациентов, страдающих саркомой Капоши;
- исходное или зарегистрированное во время терапии содержание нейтрофилов меньше 1·10 9/л у больных с ангиосаркомой Капоши.
С осторожностью его прописывают онкобольным, страдающим такими патологиями как:
- снижение уровня тромбоцитов (ниже 100·10 9/л);
- нарушение в работе печени легкой и умеренной тяжести;
- инфекции в острой стадии, в том числе вызванные вирусом герпеса;
- угнетение костномозгового кроветворения;
- тяжелое течение ишемического поражения сердца;
- аритмия;
- пережитый инфаркт миокарда.
Побочные эффекты
На фоне лечения препаратом могут наблюдаться следующие нежелательные реакции со стороны системы:
- Кроветворения: миелосупрессия; снижения количества нейтрофилов, гемоглобина, тромбоцитов, лейкоцитов; кровотечения; нейтропеническая лихорадка; миелодиспластический синдром; острый нелимфобластный лейкоз;
- Обмена веществ: синдром распада опухоли.
- Слуховой: тугоухость; звон в ушах; головокружение.
- Нервной: нейротоксичность; периферическая и вегетативная нейропатия; судороги; цефалгия; нарушения координации движения; энцефалопатия.
- Зрительной: повреждения зрительного нерва; глазная мигрень; желтое пятно; фотопсия; появление мушек перед глазами.
- Дыхательной: диспноэ; дыхательная недостаточность; эмболия легочной артерии; фиброз легкого; скопления жидкости в плевральной полости; интерстициальное воспаление легких; кашель.
- Опорно-двигательного аппарата: суставная и мышечная боль; системная красная волчанка.
- Сердечно-сосудистой: кардиомиопатия; гипотония или гипертония; “приливы”; урежение или учащение сердцебиения; шок; инфаркт миокарда; флебит и тромбофлебит; атриовентрикулярная блокада и обморок; тромбоз вен; сердечная недостаточность; фибрилляция желудочков.
- Пищеварения: жидкий стул; запор; стоматит; рвота; тошнота; эзофагит; ишемический и псевдомембранозный колит; воспаление поджелудочной железы; кишечная непроходимость; разрыв стенок кишечника; некроз печени; полный отказ от еды; тромбоз брыжеечной артерии; брюшная водянка; печеночная энцефалопатия, которая может стать причиной гибели пациента.
- Иммунной: высыпания; отек Квинке; анафилаксия; озноб; чрезмерное потоотделение; генерализованная крапивница.
- Кожных покровов и подкожной клетчатки: патологическое выпадение волос; обратимые изменения ногтей и кожи; злокачественная экссудативная эритема; мультиформная эритема; дерматит; отслоение ногтей от ногтевого ложа; склеродермия.
Кроме этого, на фоне терапии возможно развитие инфекционных заболеваний, которые могут закончиться гибелью пациента, местные реакции, такие как отек, болезненные ощущения, покраснение и уплотнение, кровоизлияние в месте введения препарата.
Во время лечения может страдать общее самочувствие: повыситься температура, развиться периферические отеки, бессилие.
Лабораторные анализы могут показать повышение активности печеночных энзимов, уровня билирубина и креатинина.
Особые указания
Лечение обязательно проводить под контролем специалиста, у которого есть опыт применения противоопухолевых средств.
При появлении диспноэ, падении давления, развитии генерализованной крапивницы, ангионевротического отека после введения “Паклитаксела”, стоит прекратить и назначит симптоматическое лечение. Вводить медикамент повторно не следует.
Во время введения препарата нужно контролировать кровяное давление, пульс и дыхание.
При развитии тяжелых нарушений предсердно-желудочковой проводимости, надо проводить соответствующую терапию, а при последующем введении медикамента нужно постоянно делать мониторинг сердца.
При развитии тяжелой формы периферической невропатии при вторичном введении дозировку лекарственного препарата стоит уменьшить на 20%.
В ходе терапии нужно постоянно контролировать уровень форменных элементов клеток крови через малые интервалы времени.
Помощь при передозировке
При передозировке у пострадавшего развиваются следующие симптомы:
- мукозит (токсико-воспалительное заболевание слизистой рта и подслизистой ткани);
- периферическая нейротоксичность;
- миелосупрессия (уменьшение количества образующихся в костном мозге клеток крови).
Специфического антидота не существует. Пострадавшему назначают препараты устраняющие признаки интоксикации.
Условия продажи, цена, аналоги
Приобрести препарат можно строго по рецепту врача. В продаже можно встретить противоопухолевое средство различных производителей:
- “Биолек”;
- “Тева Прайвэт Ко”;
- “Pliva”;
- “Фармахеми Б.В.”;
- “EBEWE PHARMA Ges.m.b.H.Nfg.KG.”.
Стоимость препарата в аптеках начинается от 577 рублей.
Кроме этого, в продаже можно встретить аналоги медикамента:
- “Митотакс”;
- “Таксол”;
- “Интаксел”.
Подбирать аналог должен только специалист!
Самолечение препаратом “Паклитаксел” недопустимо, только врач может подобрать адекватную схему терапии.
Источник