Методика лечения рака молочной железы her

Процессы роста и размножения всех клеток в организме находятся под жестким регулирующим контролем генов, которые способных запускать или останавливать их. В норме в организме поддерживается баланс между появлением новых клеток и гибелью старых. В опухолевых клетках процессы размножения клеток выходят из под контроля. Зачастую это происходит по причине возникновения «сбоев» в работе определенных генов, играющих наиболее важную роль в контроле над делением клеток.
HER2 (аббревиатура от английского human epidermal growth factor receptor 2 – рецептор фактора роста эпидермиса) является одним из таких генов. Этот ген может также обозначаться как «HER2-neu» или «ERBB2», эти названия являются синонимами. Его неправильная работа обнаруживается во многих случаях развития рака молочной железы и приводит к активной выработке в клетках одноименного белка (HER2), что заставляет клетки быстро делиться. Когда в клетке образуется избыточное количество белка HER2, говорят об амплификации этого гена. Амплификация HER2 обнаруживается примерно у 25% пациенток с диагнозом рака молочной железы. Её наличие приводит к повышению агрессивности опухолевых клеток. Вследствие высокой важности знания HER2-статуса опухоли, определение наличия амплификации HER2 является или избыточной выработки белка HER2 является одним из стандартных методов обследования, и проводится у всех пациенток с диагнозом рака молочной железы. Кроме того, в ряде исследований была продемонстрирована клиническая значимость выработки HER2 при раке желудка, по этой причине препараты, подавляющие активность этого белка также применяются для лечения рака желудка.
В чем особенности HER2-положительного рака молочной железы?
Изначально HER2-позитивный рак молочной железы был одним из наиболее агрессивных разновидностей этого заболевания, который характеризовался очень быстрым темпом роста опухоли, высоким риском развития рецидива болезни и появления отдаленных метастазов. Тем не менее, в настоящее время разработано множество препаратов, подавляющих активность этого белка (см. ниже). Они продемонстрировали высокую эффективность в лечении HER2-положительного рака молочной железы, превратив этот подтип рака в один из относительно благоприятных вариантов заболевания. Проведение целенаправленной («таргетной») терапии, блокирующей активность HER2, позволяет значительно повысить эффективность лечения и резко снизить риск развития рецидива рака молочной железы или добиться длительного контроля над болезнью в случае лечения её поздних стадий.
Кому назначаются препараты, блокирующие активность HER2?
Необходимо отметить, что применение препаратов, блокирующих активность HER2, целесообразно только в том случае, если в опухоли есть повышенная выработка этого белка вследствие наличия амплификации гена HER2. Если она отсутствует, раковые клетки не вырабатывают этот белок, следовательно, назначение препаратов, блокирующих активность этого белка не приведет к желаемому результату. По этой причине перед началом лечения всем пациенткам с диагнозом рака молочной железы перед началом лечения проводится специальное обследование, направленное на определение повышенной выработки HER2. Эта информация критически важна для правильного лечения рака молочной железы.
Как определяется HER2 статус опухоли?
В процессе диагностики рака молочной железы небольшой кусочек опухолевой ткани путем биопсии забирается для проведения иммуногистохимического исследования. Как правило, одновременно проводится определение наличия экспрессии (выработки) опухолевыми клетками рецепторов женских половых гормонов, HER2-статуса опухолевых клеток, а также темпов её роста (индекс Ki-67). При проведении этого исследования на опухолевые клетки наносятся специальные «красители», которые окрашивают HER2 в случаях, когда он содержится в клетках в большом количестве. Иммуногистохимическое исследование оценивает наличие гиперпродукции белка HER2 опухолевыми клетками.
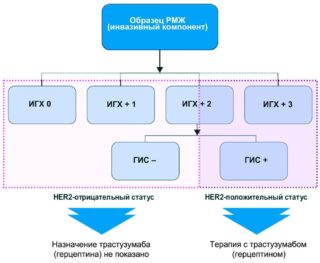
По результатам иммуногистохимического определения HER2 статуса опухоли может быть получен один из следующих результатов:
0 баллов – в опухоли не отмечено признаков экспрессии HER2 (результат исследования отрицательный, назначение анти-HER2 препаратов нецелесообразно);
1+ — в опухолевых клетках обнаружена незначительная экспрессия HER2 (результат исследования отрицательный);
2+ — в опухолевых клетках обнаружена умеренная экспрессия HER2 (результат сомнительный, требуется проведение дополнительного исследования, см. ниже);
3+ — в опухолевых клетках обнаружена повышенная экспрессия HER2 (результат положительный, назначение анти-HER2 препаратов целесообразно).
Если по результатам иммуногистохимического исследования была выявлена выраженная экспрессия HER2 (3+), пациентке показано назначение препаратов, блокирующих активность этого белка, так как опухолевые клетки активно вырабатывают этот белок и процессы их роста зависят от его функционирования. Если результат исследования отрицательный (0 или 1+) назначение такого лечения не приведет к желаемому результату.
Получение сомнительного результата (2+) означает, что по результатам иммуногистохимического исследования достоверно определить наличие экспрессии HER2 не удалось и необходимо проведение дополнительных методов исследования, например, т.н. «флюоресцентной гибридизации in situ» (FISH) или схожего с ней метода CISH. Эти методы позволяют напрямую оценить наличие амплификации HER2. По результатам проведения этих тестов может быть получен положительный или отрицательный ответ. Положительный ответ означает, что была выявлена амплификации HER2 и целесообразно назначение анти-HER2 терапии.
Какие существуют лекарственные препараты для лечения HER2-позитивного рака молочной железы?
На данный момент разработано и внедрено в клиническую практику 4 препарата, подавляющих активность HER2. Они несколько различаются по структуре и механизму действия, а также по показаниям к применению, эти лекарства могут назначаться как в комбинации с другими препаратами, например химиотерапевтическими агентами, так и самостоятельно (в монотерапии). В этом разделе представлено краткое описание этих препаратов.
Трастузумаб – лекарственный препарат, который представляет собой белок (моноклональное антитело), сконструированный таким образом, чтобы избирательно связываться с HER2 и «закрывать» его, не давая ему возможности нормально функционировать и провоцировать процессы роста и деления опухолевых клеток. Трастузумаб является препаратом, который наиболее часто назначается пациенткам с HER2-положительным раком молочной железы. Он применяется в сочетании с химиотерапией в качестве пред- или послеоперационной терапии данного заболевания, а также для первоначального лечения поздних его поздних стадий. Препарат выпускается как в виде раствора для внутривенных капельных введений, так и в виде раствора для подкожных введений. Трастузумаб-эмтанзин (T-DM1) – комбинированный препарат, который содержит молекулы трастузумаба, соединенные с противоопухолевым препаратом эмтанзином, который оказывает губительное действие на клетки. Препарат сконструирован таким образом, что молекулы трастузумаба связываются со своей мишенью на поверхности опухолевых клеток, после чего эмтанзин проникает в них и вызывает гибель раковых клеток. Помимо лечения рака молочной железы трастузумаб также применяется для лечения рака желудка в случае выявления в опухоли гиперэкспрессии HER2. Препарат вводится внутривенно капельно.
Пертузумаб – также как и трастузумаб, пертузумаб представляет собой моноклональное антитело к HER2, однако в отличие от трастузумаба он связывается с другим участком этого белка. Препарат назначается в комбинации с трастузумабом и позволяет повысить эффективность лечения. Препарат вводится внутривенно капельно.
Лапатиниб – препарат, блокирующий сигнальный путь, который проводит сигналы от HER2. Препарат применяется для лечения пациенток, у которых было отмечено прогрессирование на фоне применения режимов лечения с использованием трастузумаба, а также для лечения HER2-положительного гормонозависимого рака молочной железы, в этом случае лапатиниб применяется в комбинации с гормонотерапией. Препарат выпускается в виде таблеток и принимается внутрь.
Указанные препараты назначаются только пациенткам с HER2-положительными опухолями (экспрессия HER2 3+ при проведении иммуногистохимического исследования или выявленная амплификация гена при проведении FISH или схожего метода исследования).
Может ли HER2 статус изменяться в процессе проведения лечения?
Необходимо отметить, что HER2 статус опухоли может меняться в процессе проведения лечения как результат изменений, происходящих в раковых клетках. Клетки опухоли ищут способ выжить на фоне проводимой терапии и постоянно изменяются. Например, в случае, если произошел рецидив исходно HER2-положительной опухоли, во вновь выявленных опухолевых очагах может отмечаться исчезновение выработки этого белка и утрата зависимости опухолевых клеток от влияния этого гена. Возможно и обратное – появление гиперэкспрессии HER2 в опухолях, которые исходно не вырабатывали этот белок. По этой причине в случае развития рецидивов или появления метастазов врач может рекомендовать повторное проведение биопсии и проведение нового тестирования для определения HER2 статуса опухоли.
Источник:
- BreastCancer.org. HER2 Status.
Источник
При подозрении на злокачественное образование женщинам назначают анализ молочной железы на her2-статус. В ходе исследования определяется количество человеческого рецептора эпидермального фактора роста 2.
Что такое рецепторы her2
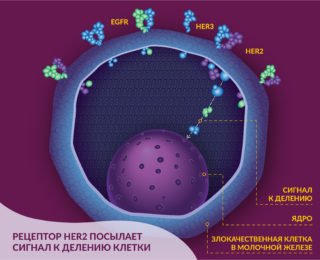 Рецептор HER 2 представляет собой трансмембранный белок. В норме этот фермент позволяет регулировать сигнал деления и жизненный цикл клеток. Однако при гиперэкспрессии происходит его мутация, соответственно начинает развитие злокачественное новообразование. Гиперэкспрессия довольно детально изучена на примере молочных желез у женщин, ее связь с канцерогеном зачастую имеет положительный тип рецептора. Кроме того, его наличие в организме считается главным онкологическим маркером при обследовании РМЖ.
Рецептор HER 2 представляет собой трансмембранный белок. В норме этот фермент позволяет регулировать сигнал деления и жизненный цикл клеток. Однако при гиперэкспрессии происходит его мутация, соответственно начинает развитие злокачественное новообразование. Гиперэкспрессия довольно детально изучена на примере молочных желез у женщин, ее связь с канцерогеном зачастую имеет положительный тип рецептора. Кроме того, его наличие в организме считается главным онкологическим маркером при обследовании РМЖ.
Обследование при подозрении прогрессирования опухоли обязательно включает проверку HER2. На основании полученных данных специалистам удается выяснить дальнейший прогноз после лечения, а также выживаемость.
HER 2 позитивный отличается повышенной агрессивностью и ростом. В отличие от негативного типа. Однако, первый вариант рецептора лучше поддается лечению химиопрепаратами. При негативном диагнозе данная терапия считается бессильной.
Как определить her2 статус
Когда проверяется her2-статус 1, происходит выявление повышенного уровня белоксодержащих рецепторов человека при раке молочной железы. Для этой цели выполняют тестирование тканей опухоли, которые берутся у пациентки с помощью биопсии. Определяется несколькими способами.
- Иммуноцитохимическое исследование или ИГХ. Методика недорогая, но достаточно информативная. С помощью гистологических клеток удается определить количество HER 2 протеина в раковых новообразованиях, проявившихся в молочных железах. Для данных целей применяются специальные красящие вещества. Если краситель стал ярким и контрастным, количество рецепторов увеличено. Данный показатель принято анализировать по шкале от 0 до 3.
- Флуоресцентная гибридизация или FISH. Считается наиболее точным исследованием при выявлении позитивного HER 2 статуса. В результате рак молочной железы разделяют по группам: her2 негативный рак молочной железы, her 2 позитивный рак.
- SPOT-LIGHT HER 2 CISH. Данный тест выявляет степени амплификации гена. Полученные результаты тестов делятся подобным образом: позитивный рак (с присутствием амплификации), негативный (без амплификации).
- Inform HER2 Dual ISH — один из новых тестов определения раковых клеток. Результаты делятся как и в предыдущих методах исследования. Данный анализ считается усовершенствованным и дает точную характеристику и подтверждение злокачественности новообразования.
Положительный тест HER 2 говорит о том, что РМЖ ведет себя агрессивно и способен быстро метастазировать в другие органы. Заболеванию подвержены пациентки в репродуктивном возрасте.
Роль анализа в лечении рака
 HER 2 является протоонкогеном, влияет на продуцирование клеток белка. В норме происходит регуляция, но некоторые отклонения провоцируют появление клеток злокачественного характера. Благодаря данной тактике исследования и новым технологиями в сфере биологии удается своевременно, а главное правильно назначить корректное лечение.
HER 2 является протоонкогеном, влияет на продуцирование клеток белка. В норме происходит регуляция, но некоторые отклонения провоцируют появление клеток злокачественного характера. Благодаря данной тактике исследования и новым технологиями в сфере биологии удается своевременно, а главное правильно назначить корректное лечение.
В ходе назначенной терапии при раке молочных желез у женщин возможно изменение статуса Her 2, что считается результатом. Медики отмечают, что клетки опухоли обладают высокой жизнеспособностью, чтобы выжить при введении химикатов в организм, они подвергаются изменению.
Также возможно усиление прогрессирования опухоли, клетки могут начать вырабатывать белок, если ранее не производили эту функцию. Поэтому с целью контролирования состояния опухоли данный тест проводится регулярно.
Особенности терапии
 Лечение хер-положительных опухолей груди в медицинской практике осуществляется с помощью небольшого спектра препаратов. Они считаются действующими при определении агрессивного рецептора в организме. Лекарственные средства различаются по механизму действия.
Лечение хер-положительных опухолей груди в медицинской практике осуществляется с помощью небольшого спектра препаратов. Они считаются действующими при определении агрессивного рецептора в организме. Лекарственные средства различаются по механизму действия.
Пертузумаб
В препарате содержится моноклинальное антитело, которое способно осуществлять активную борьбу против HER 2. Препарат назначают в комплексе с другими лекарствами, чтобы повысить эффективность лечения. Вводится внутривенно с помощью капельниц.
Трастузумаб
 В качестве действующего вещества данного препарата выступает белок. Он сконструирован специальным способом, воздействует на клетки мутированных генов, останавливает их рост и дальнейшее распространение опухоли. Применяется в предоперационный и реабилитационный периоды.
В качестве действующего вещества данного препарата выступает белок. Он сконструирован специальным способом, воздействует на клетки мутированных генов, останавливает их рост и дальнейшее распространение опухоли. Применяется в предоперационный и реабилитационный периоды.
Умеренная физическая нагрузка, например, трехчасовая ходьба положительно влияет на лечение рака. Данная методика позволяет усилить функцию иммунитета.
Лапатиниб
 Данное лекарственное средство предназначено для купирования сигналов, переходящих от раковых клеток к здоровым. Подходит для терапии гормонозависимой положительной патологии молочной железы. Препарат назначается в форме таблеток по индивидуальному курсу. Показан в комбинации с гормональными аптечными препаратами.
Данное лекарственное средство предназначено для купирования сигналов, переходящих от раковых клеток к здоровым. Подходит для терапии гормонозависимой положительной патологии молочной железы. Препарат назначается в форме таблеток по индивидуальному курсу. Показан в комбинации с гормональными аптечными препаратами.
Перечисленные препараты прописываются пациенткам, у которых обнаружена экспрессия HER 2 +3 и положительный тип генной мутации опухоли.
Виды ремиссии при опухоли молочной железы
Ремиссия при хер-положительном РМЖ представляет собой период, когда все признаки злокачественности начинают отступать и пациентка идет на поправку. Однако нельзя считать, что патология полностью исключена. Онкологические опухоли способны рецидивировать. Поэтому главное в период реабилитации – своевременно проходить обследование.
- Полная ремиссия. Отличается полным отступлением симптомов онкологии и уменьшением опухоли в размерах.
- Неполная. Говорит о том, что женский организм все еще находится под угрозой, поэтому необходимо продолжать лечение.
- Спонтанная. Данный вид малоизучен в медицине, поэтому считается неблагоприятным и подозрительным. Зачастую признаки онкологической патологии полностью или частично исчезают без применения специальной терапии.
Ремиссия может оказаться недостоверным методом определения этапа заболевания.
Особенности негативного Her
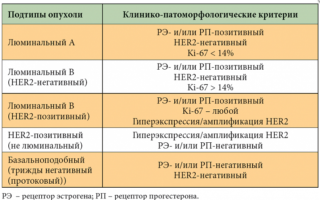
Подтипы рака и их клинико-патоморфологические критерии
В результате поздней диагностики чаще всего рак молочной железы определяется как негативный. Выделяют несколько иммунногистохимических подтипов:
- А и В-люминальный;
- негативный тройной.
Негативный тройной рак зачастую имеет благоприятный прогноз. В данном случае выделяют слизистый, тубулярный, медуллярный.
Рецидив рака молочной железы
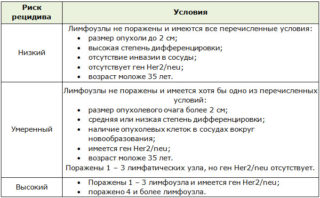
Вероятность развития рецидива
Вероятность повторного развития заболевания зависит от того, насколько было выраженным первичное прогрессирование. Чтобы избежать рецидива, пациентки идут на разные меры:
- частичное или полное удаление пораженной молочной железы;
- прием сильнодействующих препаратов;
- прохождение гормональной терапии.
Чтобы своевременно выявить рецидивирующий рак, проходят инструментальную диагностику каждые 5 месяцев. Обычно her2 позитивный рак молочной железы имеет хороший прогноз и 75% выживаемость.
Отзывы о лечении хер-положительного рака груди говорят об эффективности терапии только при условии ее своевременного начала.
Как предупредить развитие РМЖ
 Существует масса рисков, которые влияют на развитие онкологической патологии молочной железы. Однако можно снизить вероятность проявления злокачественного новообразования некоторыми способами.
Существует масса рисков, которые влияют на развитие онкологической патологии молочной железы. Однако можно снизить вероятность проявления злокачественного новообразования некоторыми способами.
- Физическая активность. Умеренная нагрузка на организм и пешие прогулки способствуют выработке иммунитета и выздоровлению.
- Ранние роды. Женщинам желательно испытать роль материнства до 35 лет. В противном случае есть вероятность развития гормональных нарушений, влияющих на появление РМЖ.
- Слежение за собственным весом. Ожирение неблагоприятно влияет на состояние организма, для него это колоссальная нагрузка, поэтому исход — рак груди.
- Ограничение вредных привычек: табакокурение и спиртные напитки убивают здоровые клетки в организме, провоцируют развитие их мутации.
Самое главное – не заниматься самолечением и не применять без надобности гормональные средства. Они могут вызвать сбой в работе эндокринной системы, что негативно сказывается на здоровье женской груди.
Источник
Работа, опубликованная в Nature Medicine учёными из National Cancer Institute (NCI), описывает новый тип иммунотерапии, который привёл к полному исчезновению опухолей у женщины с метастатическим раком молочной железы, которой осталось всего несколько месяцев жизни.
Результаты показывают, как естественные опухолевые инфильтрирующие лимфоциты (TIL) были извлечены из опухоли пациента, выращены вне её тела, чтобы увеличить их количество, и введены обратно пациенту для борьбы с раком. Пациент ранее получил несколько форм лечения, включая гормональную терапию и химиотерапию, но никакая из них не остановила прогрессирование рака. После лечения все опухоли пациентки исчезли, и через 22 месяца она все ещё находится в ремиссии.
Учёные с энтузиазмом относятся к возможности TIL лечить группу раковых заболеваний, называемых «common epithelial cancers», включающие в себя рак толстой кишки, прямой кишки, поджелудочной железы, молочной железы и лёгких, что составляет 90% всех случаев смерти от рака в США, около 540 000 человек ежегодно, большинство из них от метастазирования.
«Как только эти раки распространяются, большинство людей умирает. У нас нет эффективных способов устранения метастатического рака», – сказал Стивен Розенберг, MD, PhD, глава отделения хирургии Center for Cancer Research при NCI (CCR).
Первым шагом этого нового подхода к лечению является секвенирование генома опухоли. В случае этого пациента учёные нашли 62 мутации в клетках опухоли молочной железы. Второе – выделить TIL, которые присутствуют в 80% опухолей эпителиальных клеток, но в крошечных количествах, недостаточных, чтобы уничтожить опухоль. Затем они анализируются на их способность распознавать мутированные белки в опухоли. В случае с пациентом с метастатическим раком молочной железы учёные обнаружили TIL, которые распознали четыре мутантных белка.
«Мы изолируем эти лимфоциты, выращиваем их в большом количестве и возвращаем их пациентам. Мы вырастили для этого пациента около 90 миллиардов клеток», – сказал Розенберг.
Во время выращивания TIL пациента также лечили иммунотерапевтическим веществом Keytruda, блокирующим PD-1, в целях изменения иммунной системы, чтобы иные иммунные клетки не мешали TIL, когда их вводили обратно пациенту.
«Мы включаем в лечение пациентов их собственные лимфобласты, которые представляют собой природные Т-клетки, а не генно-инженерные. Это наиболее персонализированное лечение, какое только можно себе вообразить», – сказал Розенберг.
Пациент с метастатическим раком молочной железы – не единственный человек, успешно прошедший лечение с использованием этого метода. Розенберг и его коллеги также достигли впечатляющих результатов при использовании TIL в лечении ещё трёх различных типов метастатического рака: колоректального, желчных протоков и шейки матки.
«Эти методы лечения способны лечить пациентов с любым раком», – утверждает Розенберг.
Хотя результаты, несомненно, являются многообещающими, особенно из-за низкого уровня токсичности, испытываемого пациентами по сравнению с химиотерапиями, рак часто развивает устойчивость к лечению, и часто метастазы могут иметь мутации, отличные от начальной опухоли.
Так легко ли у пациентов разовьётся устойчивость к TIL?
«По иронии, именно те мутации, которые вызвали рак, могут быть ахиллесовой пятой, которая позволяет уничтожить рак. Очень важно нацеливать сразу на несколько мутаций», – сказал Розенберг.
Как ни странно, это одно из преимуществ многих старых химиотерапевтических препаратов по сравнению с новыми персонализированными методами лечения. Из-за того, что химиотерапии без разбора пронизывают геном повреждениями в стиле ковровой бомбардировки, раковой клетке становится сложнее выработать устойчивость к ним. Выбор TIL, которые нацелены на небольшое количество мутированных белков в опухоли, может увеличить вероятность, что рак сможет развить резистентность. Нужны ещё работы в этой сфере, а также приёмы по изучению какие мутации у раковых клеток являются возможными мишенями TIL.
Если крупные работы подтверждают эти великолепные предварительные результаты, разработка персонализированной терапии пациенту, несомненно, является финансовой и технической проблемой, требующей специализированных лабораторий и опыта. Насколько практично производить полностью персонализированную терапию?
«Люди говорили это и о CAR Т клетках. Если вы найдёте что-то, что работает на пациентах, сложно это или нет, инженерный гений найдёт способ заставить это работать», – сказал Розенберг.
И несколько компаний уже проводят испытания лечения TIL, в том числе Bristol-Myers Squibb и Iovance Biotherapeutics, последняя из которых специально фокусируется на TIL. В настоящее время проводятся клинические испытания TIL для меланомы, рака шейки матки, лёгких и даже, как известно, мало поддающихся лечению глиобластомы и рака поджелудочной железы.
«Это изменение нашего мышления, что может быть нужно в лечении этих типов рака. Новая парадигма лечения рака», – сказал Розенберг.
Нечасто в борьбу вступают совершенно новые методы лечения рака с такими впечатляющими результатами, как показанные TIL в этих примерах. Что сейчас крайне нужно, так это результаты более масштабных клинических испытаний и постоянного контроля за пациентами, которые были успешно вылечены, чтобы убедиться, что у них не возникло проблем.
«Это иллюстративный пример, который ещё раз показывает нам силу иммунотерапии», – сказал Том Мистели, PhD, глава CCR в NCI. «Если это подтвердится в более широком масштабе, оно обещает ещё больше расширить сферу применения этой Т-клеточной терапии для более широкого спектра раковых заболеваний».
Источник