Лечение зубов после лучевой терапии
Дмитриева Е.Ф.,
врач-стоматолог, ООО «ТалисманДент М», г. Челябинск
Нуриева Н.С., д.м.н.,
доцент кафедры ортопедической стоматологии ЮУГМУ
Во всем мире рак головы и шеи составляет около 10% всех злокачественных новообразований [1]. Лечение злокачественных новообразований головы и шеи требует мультидисциплинарного подхода, сотрудничества врачей различных специальностей: хирурга-онколога, радиолога, химиотерапевта, рентгенолога, эндоскописта, стоматолога, патоморфолога, цитолога, а также врачей некоторых других специальностей, каждый из которых участвует в установлении диагноза, оценки степени распространения опухоли, выработке тактики лечения и его проведении [2]. Выбор стратегии и лечения в основном осуществляется между хирургическим лечением, лучевой терапией и комбинированными методами.
Лучевая терапия – метод лечения с использованием ионизирующего излучения. Среди различных методов лечения в клинической онкологии лучевая терапия занимает одно из ведущих мест. По данным ВОЗ, 70-75% онкологических больных нуждаются в проведении лучевой терапии. Облучение может быть радикальным, паллиативным или используется в комбинации с операцией. К преимуществам лучевой терапии следует отнести ее хорошую переносимость, возможность достижения в ранних стадиях некоторых опухолей стойкого излечения с сохранением функции пораженного органа. Применение лучевого лечения в качестве паллиативной, самостоятельной терапии в неоперабельных случаях является самым эффективным среди других лечебных мероприятий.
В лучевой терапии органов головы и шеи в самостоятельном плане для получения радикального или паллиативного эффекта широко применяется подобранный ритм ежедневного облучения по 2 г (5 раз в неделю; за неделю – 10 г). Суммарная очаговая доза при этом составляет (при средней радиочувствительности опухоли) 60-70 г. Лучевая терапия проводится по расщепленной программе: первый курс – до суммарной очаговой дозы 30 г, затем следует перерыв в лечении на 2-3 нед. Второй курс проводится также разовой очаговой дозой 2 г до суммарной очаговой дозы 40 г (общая суммарная доза – 70 г) [3].
Однако проблемой при этом остается довольно высокая частота тяжелых посттерапевтических осложнений, существенно снижающих возможности метода лечения. Частым осложнением лучевой терапии является лучевое поражение зубов (рис. 1).
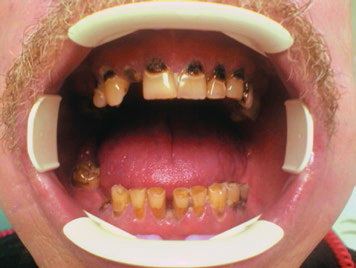
Рис.1. Лучевой некроз зубов после курса лучевой терапии (54 г)
Одним из перспективных направлений в этом плане является использование современных технических достижений, позволяющих снизить объем нежелательно облучаемых нормальных тканей с концентрацией максимальной дозы излучения на уровне опухоли и на этой основе улучшить результаты лечения этого контингента больных [4].
С целью повышения эффективности лучевой терапии обосновано применение режимов гиперфракционированного облучения. По мнению некоторых отечественных и зарубежных исследователей, увеличение разовой очаговой дозы до 2,4-3 г при условии подведения последней за 2-3 фракции в сутки с интервалом между фракциями не менее 4 часов сопровождается повышением эффективности лечения рака носоглотки на 20-30% [5,6]. В исследовании, выполненным S.L. Wolden и соавт., которые провели сравнительный анализ результатов облучения в обычном режиме фракционирования дозы (1,8 г/5 раз в неделю/70 г) и динамического фракционирования, когда в течение 5-й и 6-й недель проводится облучение с использованием ускоренного фракционирования разовой дозой 1,6 г 2 раза в день в сочетании с химиотерапией цисплатином. Отмечено статистически значимое увеличение частоты полной резорбции опухоли, безрецидивной и общей выживаемости [14]. По результатам исследований ряда авторов, ранние лучевые повреждения со стороны слизистой оболочки встречались значительно чаще при гиперфракционировании. Однако число поздних лучевых повреждений было одинаковым [7].
Не меньшее значение уделяется качеству проведения лучевой терапии. Применение особых приспособлений (подголовники, маски из термоплавких пластмасс), фиксирующих определенное положение больного в процессе облучения, индивидуальное дозиметрическое планирование на основе рентгеновской компьютерной томографии и формирование динамически изменяющихся фигурных полей облучения с помощью мультилифтного коллиматора способствуют повышению эффективности лучевой терапии. В сравнении со стандартной программой лучевой терапии применение методики конформного облучения на основе трехплоскостного планирования позволяет создать оптимальное соотношение между дозой излучения, подводимой к опухоли и в окружающих тканях [8].
Лучевые поражения твердых тканей зуба при длительном воздействии на организм малыми дозами зависят от суммарной дозы, облучения, интенсивности облучения и фактора времени. Изменения в тканях зуба проявляются в виде меловых пятен, пигментации, размягчения и некроза эмали и дентина (рис. 2).
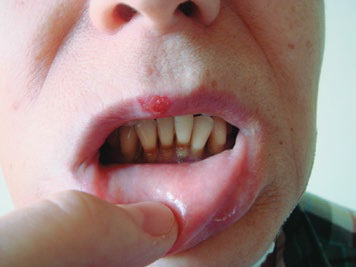
Рис.2. Лучевой кариес после сплит-курса лучевой терапии
Большие дозы облучения могут приводить к некрозу больших участков эмали и дентина в области иммунных зон зубов. Изменения в пульпе проявляются в виде гиалинизации стенок сосудов, вакуольного и жирового перерождения, атрофии и дегенерации одонтобластов и т.д. Комплекс патоморфологических изменений в тканях зуба при этих поражениях во многом напоминает кариес зубов, что дало основание ввести термин лучевой кариес.
Лучевой кариес зуба – (c. dentis radialis) генерализованный кариес зуба, развивающийся как осложнение рентгено- или радиотерапии челюстно-лицевой области; протекает с пигментацией и размягчением поверхностных слоев и образованием глубоких пришеечных полостей.
До настоящего времени не разработано единое мнение по поводу механизма и характера изменений в тканях зуба и полости рта вследствие радиационного излучения.
Иванова Л.А. считает, что возникающие под влиянием ионизирующего излучения распад белковых молекул, нарушения обменных процессов, расстройства кровообращения, гипоксия в совокупности способствуют развитию неблагоприятных условий существования пульпы, и чем дольше они будут иметь место, тем более тяжелыми могут быть последствия как для пульпы, так и для твердых тканей зуба [9]. По мнению Барер Г.М., Иванчиковой Л.А., в основе изменений твердых тканей лежат повреждения белковой матрицы и нарушение химической связи между минеральной и белковой фракциями. Уже в процессе облучения авторы наблюдали в дентине и цементе зубов экспериментальных животных деминерализацию и деструктивные изменения, что можно объяснить особенностями гистологического строения твердых тканей, чрезвычайно низким обменом веществ в них, неспособностью тканей к восстановлению [10].
По данным Окадо Ш., 1979, дальнейшее развитие возникших во время облучения изменений дентина, характеризующиеся продолжающейся деминерализацией, увеличением очагов деструкции, разрушением эмалево-дентинного соединения, появлением лакунарного рассасывания дентина на границе с пульпой объясняется как реакцией последствия, так и влиянием поврежденной пульпы, восстановление которой после облучения является неполным. В разрушении эмалево-дентинного соединения имеет значение различие в интенсивности деминерализации эмали и дентина. Насыщенность минеральными веществами дентина снижается в значительно большей степени, чем эмали, что приводит к дезинтеграции этих тканей.
Иванова Л.А., Боровский Е.В., Сегень И.Т. и Назаров Г.И. указывают, что патологический процесс возникает одновременно во многих зубах, распространяется вокруг шеек и по поверхностям коронок, заканчиваясь, как правило, отломом зуба на уровне десневого края. Авторами обращается внимание на неэффективность пломбирования из-за появления вокруг пломб, а также в ранее неповрежденных участках новых дефектов [9, 11, 12].
Изменения на слизистой оболочке полости рта, на что указывает Щелканогова М.Г. и соавт., 1993, плохая гигиена в комплексе приводят к нарушению самоочищения зубов, на поверхности эмали создается критическая ситуация (pH 4-5 под налетом), благоприятствующая деминерализации облученной эмали. Повышается чувствительность зубов к изменениям температуры, к давлению, к сладкому и кислому, изменяется цвет (до светло- или темно-серого), эмаль теряет блеск, становится ломкой хрупкой; зубы покрыты толстым клейким трудноудаляемым налетом. Появляется кариесогенная микрофлора. Кариес возникает и на сравнительно редко поражаемых участках (в области бугров, на режущих отделах). Наиболее характерен пришеечный кариес передних зубов. Процесс протекает безболезненно, быстро прогрессирует и заканчивается отломом коронок.
Принципы профилактики и лечения отражены в протоколе Dental Disease Section/International Society of Oral Oncology (ISOO) (2010):
1. Применение фторидсодержащих препаратов. Реминерализующая терапия значительно снижает риск развития патологии твердых тканей зубов (Level of Evidence: II, Grade of Recommendation: B), (рис. 3).
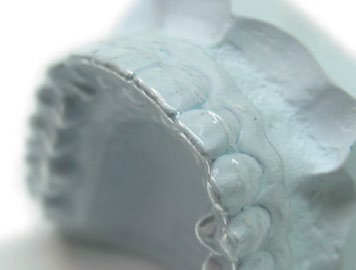
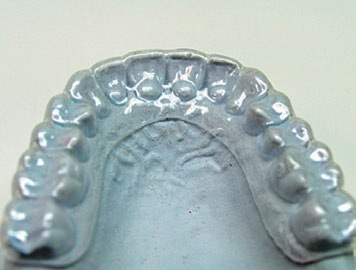
Рис.3. Каппы для реминерализующей терапии
2. Применение полосканий для полости рта с хлоргексидином. Использование этих препаратов улучшает гигиеническое состояние полости рта, а также способствует снижению числа Streptococcus mutans. При назначении хлоргексидин содержащих полосканий необходимо принимать к сведению возможность возникновения таких побочных эффектов как окрашивание зубного камня и изменение вкусовой чувствительности (Level of Evidence: II, Grade of Recommendation: B).
3. Восстановление дефектов твердых тканей зубов. Для восстановления дефектов твердых тканей зубов рекомендуется использовать композитные материалы, гибридные стеклоиономерные цементы и амальгаму. Применение традиционных СИЦ менее предпочтительно (Level of Evidence: II, Grade of Recommendation: B) [13].
При поражении твердых тканей коронки зуба лечение проводят в несколько этапов. Вначале осторожно удаляют некротические массы из дефектов зубов вручную экскаватором, чтобы не внедриться в полость зуба, а затем вводят кальцифицирующую пасту, состоящую из равных частей порошка глицерофосфата кальция, оксида цинка и глицерина. Пасту накладывают тонким слоем на дно и стенки образовавшейся полости и закрывают временным пломбировочным материалом.
Следующий этап отсроченного лечения зубов проводят через 1-1,5 мес. Он состоит в удалении нежизнеспособных, некротизированных тканей зуба при помощи бора до минерализованного участка дентина или эмали, после чего вновь накладывают кальцифицирующую пасту и пломбируют зубы стеклоиономерными цементами.
При более глубоких поражениях устраняют имеющиеся некротические дефекты стеклоиономерными цементами и через 3-4 месяца, если этого требует косметическая реставрация передних зубов, часть стеклоиономера удаляют, а сверху накладывают композитный пломбировочный материал.
Таким образом, лучевой кариес является распространенным осложнением лучевой терапии рака орофарингеальной зоны. На сегодняшний день разнятся мнения о клинической картине, особенностях течения заболевания и тактике лечения. Нами не найдены данные в литературе о зависимости режимов фракционирования и лучевыми повреждениями зубов в ранние и отдаленные сроки, а также о влиянии конформного облучения на твердые ткани зуба. Планируем более детальное изучение проблемы.
Список литературы:
1. Черенков В.Г. Клиническая онкология: учеб. пособие для системы постдиплом. образования врачей / В.Г. Черенков. – Изд. 3-е, испр. и доп. – М.: МК, 2010. – 434 с.
2. Кропотов М.А. Общие принципы лечения больных первичным раком головы и шеи / М.А. Кропотов // Практическая онкология. – 2003. – Т.4, №1. – С.1-7.
3. Онкология: учебник для вузов / Вельшер Л.З., Матякин Е.Г., Дудицкая Т.К., Поляков Б.И. – 2009. – 512 с.
4. Алиева С.Б. Химиолучевая терапия больных с местнораспространенным плоскоклеточным раком головы и шеи/ С.Б.Алиева // Практическая онкология. – 2008. – Т.9, №1. – С.27-30.
5. Алиев Б.М., Гарин А.М., Кошалиев Э.Ш. Сравнительная оценка эффективности лучевого и химиолучевого лечения местнораспространенного рака носоглотки III-IV стадиями заболевания // Мед. радиол. – 1987. – №7. – С. 25-30.
6. Алиев Б.М., Гарин А.М., Чуприк-Малиновская Т.П. Рак носоглотки: опыт лучевого и химиолучевого лечения // Вестн. ОНЦ РАМН. – 1995. – №1. – С. 26-32.
7. Канаев С.В. Лучевая терапия злокачественных опухолей головы и шеи/ С.В.Канаев // Практическая онкология. – 2003. – Т.4, №1. – С. 15-24.
8. Чуприк-Малиновская Т.П. Рак носоглотки: вопросы диагностики и лечения // Практическая онкология. – 2003. – Т.4, №1. – С. 38-44.
9. Иванова Л.А. Профилактика постлучевых поражений зубов.//Методические рекомендации. – Пермь, 1987.
10. Барер Г.M. Изменения ультраструктуры твердых тканей зубов после местного облучения // Г. М. Барер, Л. А. Иванчикова; Г. И. Назаров // Стоматология. 1977. – №1. – С. 4-7.
11. Боровский Е.В., Сазонов Н.И. Изменение проницаемости эмали зубов после дистанционного гамма-облучения нижней челюсти // Стоматология. – 1978. – С.1-5.
12. Назаров Г.И. Изменение зубов и челюстей после локального гамма-облучения // Мед. радиология. – 1975. – №8. – С.75-76.
13. Боровский Е.В. Реставрация лучевого кариеса зубов. Клинический пример/Е.В. Боровский, И.М. Макеева, Е.А. Скатова// Стоматология детского возраста и профилактика: рецензируемый, рекомендованный ВАК научный журнал. – 2012. – Т. XI, №2. – С.11-19.
14. Wolden S.L., Zelefsky M.J., Kraus D.H. et al. Accelerated concomitant boost radiotherapy and chemotherapy for advanced nasopharyngeal carcinoma // J. Clin. Oncol. – 2001/ – Vol. 19(4). – P. 1105-1110.
Статья предоставлена журналом «Проблемы стоматологии»
Источник
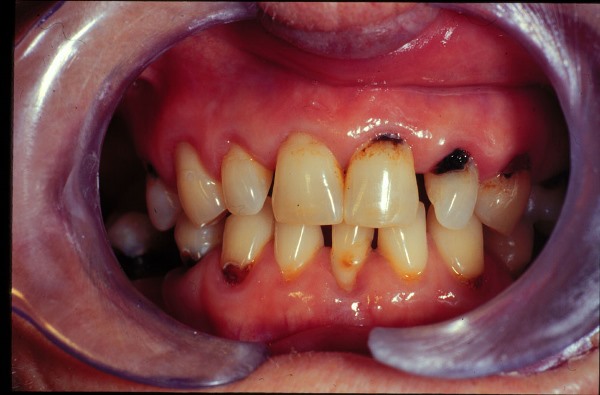
Лучевой кариес – распространенное осложнение у пациентов, получающих терапию по поводу новообразований.
До настоящего времени единое мнение медиков о механизме и характере изменений в структурах зуба после противоопухолевой терапии отсутствует.
Но есть предположение, что лучевой кариес активно развивается на фоне некариозных поражений. Об этом и других данных, расскажет статья.
Общее представление
Всех пациентов со злокачественными образованиями в анамнезе в плановом порядке наблюдают стоматологические клиники, включая ортодонтические и педиатрические практики.
Задача стоматолога тесно сотрудничать с лечащим врачом, т. к. стоматологические проблемы могут обернуться осложнениями при проведении противоопухолевой терапии органов головы и шеи у пациентов с онкогематологическими заболеваниями.
Причинно-следственную взаимосвязь между поражениями твердых тканей зубов и лучевым воздействием установить не всегда возможно. Однако раннее выявление патологий полости рта, индивидуальная гигиена и профилактика помогают снизить степень поражения элементов челюстных рядов при противоопухолевом лечении.

По статистическим данным, в облучении нуждаются 75% онкологических больных. При этом медики отмечают высокую частоту постлучевых осложнений, в разы снижающих возможность использования этого метода лечения.
При лучевой терапии ионизирующее излучение локально воздействует на зубы. Ткани костных органов полости рта поражаются, что связано не только с непосредственным негативным воздействием облучения, но с иммунодефицитом, сбоями в минерально-белковом обмене, изменением состава и количества слюны.
Противоопухолевая терапия снижает кариесрезистентность, изменяет гомеостаз ротовой жидкости, повышает опасность возникновения стоматологических аномалий, увеличивает риск образования кариозных полостей. Патофизиологические изменения в структуре зубов схожи с кариесом, что стало основанием использовать термин «лучевой кариес».
Патологический процесс, развивающийся в тканях единицы как осложнение радиотерапии, характеризуется наличием пигментации, размягчением эмали и образованием обширных пришеечных полостей.
Кариесогенная ситуация при лучевой терапии чаще возникает на фоне нарушения микрофлоры ротовой полости. Степень разрушения зависит от общей дозы облучения, его интенсивности и времени воздействия.
Причины развития и признаки
Характер и механизм патологических изменений в тканях зубов в результате радиационного воздействия до сих пор точно неясен.
Часть медиков и исследователей склоняются к мнению, что лучевые осложнения – это некариозные поражения. Но есть и те специалисты, которые уверенны, что после облучения кариес развивается наряду с некариозными поражениями.
Существует несколько предположений, объясняющих механизм зарождения и развития лучевого разрушительного процесса:
- сосудистые, морфологические, дегенеративные изменения в пульпе;
- пагубное воздействие на костные органы ксеростомии;
- иммунодепрессивное действие ионизирующего излучения;
- накопление в твердых тканях недоокисленных продуктов метаболизма вследствие нарушения аэробной фазы тканевого дыхания;
- нарушение трофики и физиологических процессов реминерализации внешней оболочки и дентина;
- сбой в нормальном функционировании слюнных желез;
- дисбаланс реминерализующего механизма в среде защитной оболочки зубов − слюна.
Доказано, что лучевое излучение негативно сказывается на тканях, органах и структурах полости рта. Рассмотрим самые достоверные факты:
- Эмаль. Стремительную деминерализацию эмали вызывает повышение pH после облучения. Единицы становятся чувствительными к нагрузкам, холодной, горячей, сладкой и кислой пище.
- Дентин. Лучевой кариес может развиваться на фоне повреждения белковой матрицы дентина. При ЛТ химическая связь между его биологическими и минеральными составляющими нарушается. Сниженный обменный процесс в костях блокирует способность к естественному восстановлению.
- Эмалево-дентинная граница. Эмалево-дентинная связь при облучении разрушается. Дезинтеграция возникает из-за разной интенсивности действия облучения на защитную оболочку и дентин.
- Пульпа. Лучевая терапия часто провоцирует развитие гиалиноза – нарушения, приводящего к поражению стенок сосудов. Это вызывает гипоксию тканей пульпы. Дентинообразующие клетки разрушаются, что оборачивается дисфункцией пульпы.
Постлучевое поражение имеет характерные проявления. Практически у всех больных диагностируются очаговые эрозии на слизистой оболочке язычной мышцы, щек, губ. Искажаются вкусовые ощущения, отмечается сухость ротовой полости.

Также к признакам негативных изменений в тканях зуба после лучевого воздействия относятся:
- меловидные пятна;
- размягчение, некроз внешней оболочки и дентина;
- пигментация;
- тусклость и ломкость эмали;
- повышенная стираемость жевательной и вестибулярной поверхности;
- наличие участков некроза.
Характерные особенности образованных полостей:
- неровные изъеденные края;
- прозрачность и хрупкость краевых линий в пределах эмали;
- наличие размягченной серой массы в полости;
- быстрое выпадение ранее поставленной пломбы.
Симптомы лучевой болезни полости рта при различных стадиях:
- Первая. В течение первых нескольких суток после облучения, язык пациента шершавый. Отмечается сухость ротовой полости. На слизистых появляются точечные кровоизлияния с матовым оттенком.
- Вторая. Стадия благополучия. Разрушительные процессы и болезненные ощущения отсутствуют.
- Третья. Запускается этап разгара заболевания. Дно ротовой полости покрывается обширными кровоизлияниями. Слизистые оболочки сильно отекают.
Начинается язвенный некроз тканей. Язвы, имеющие неровные контуры серого цвета, быстро распространяются на костные ткани и мышечные структуры. Все это может сопровождаться расшатыванием и выпадением зубов.
В процессе лучевой терапии функции одонтобластов подавляются, поэтому при кариозном поражении пациент не испытывает болезненных ощущений.
Это и является главной характерной особенностью лучевого кариеса. При данном патологическом процессе на неизмененных участках дентина присутствует хрящеподобная структура.
При лучевом кариесе у пациента может безболезненно отколоться коронковая часть.
По наблюдениям медиков, после облучения интенсивно разрушаются интактные зубы и сокращается число полноценных пломб.
Без своевременных радикальных лечебных мероприятий через год у пациента поражаются практически все зубы.
Дробное ионизирующее облучение людей обычно связано с профессиональными особенностями работы и провоцирует хроническое поражение. В этом случае на поверхности единиц появляются плоские дефекты, покрытые серой массой. Эмаль и дентин достаточно твердый. Такие поражения не вызывают болезненных и дискомфортных ощущений.
Диагностика
Интенсивность развития лучевого кариеса зависит от зоны и дозы облучения. При ионизирующем воздействии на голову, шею и плечи, врач может визуально наблюдать обширные некротические поражения зубов в ротовой полости пациента.
В других случаях кариес протекает остро и имеет определенные клинические особенности.
Правильно и быстро диагностировать лучевой кариес достаточно проблематично. Дело в том, что у многих пациентов после лучевого воздействия отсутствуют стоматологические проблемы.
Распознать ранний патологический процесс также сложно в связи с трудностями определения причинно-следственных связей, имеющих место при лечении онкологических болезней радиотерапией.
Большую значимость для медиков при определении обширности и характера осложнений после ЛТ имеет дифференциальная диагностика. Она дает возможность классифицировать кариес, определить вид, форму болезни и обособить интоксикацию фтором или врожденное недоразвитие эмали от последствий лучевой терапии.

Особенности патологий, вызванных облучением:
- Поражения наблюдаются на многих единицах и значительной площади (обычный кариес характеризуется единичными проявлениями).
- Лучевые кариозные поражения развиваются стремительно (обычный кариес сначала затрагивает эмаль и только спустя много месяцев проникает в более глубокие ткани).
Основной момент, помогающий диагностировать лучевое поражение зубов – это обследование ротовой полости пациента с целью выявления кариеса до проведения облучения.
Тактика профилактики и лечения
В лечении лучевого кариеса специалисты применяют комплексный подход. Устранение признаков заболевания проводится поэтапно.
Данный вид кариозного процесса невозможно остановить, запломбировав полость. Со временем вблизи пломбы возникают новые очаги поражения твердых тканей.
Самым действенным способом устранения разрушительного процесса считается лечение по следующему протоколу:
- Применение фторсодержащих препаратов. Цель реминерализующей фторотерапии – нормализовать баланс микроэлементов. Запустить процесс восстановления поврежденных участков.
Процедура повышает сопротивляемость тканей к вредным воздействиям. Методика основывается на нанесения на элементы челюстного ряда препаратов, содержащих кальций, фтор, цинк и фосфор.
- Полоскания с Хлоргексидином. Препарат эффективен в борьбе с большинством микроорганизмов, включая кариесогенные бактерии. Сохраняет антисептические свойства даже при контакте с кровью и гнойным экссудатом.
Раствор не вызывает раздражения слизистой оболочки ротовой полости, т. к. может использоваться в невысокой концентрации.
- Восстановление дефектов.
Реставрация пораженных единиц проводится в несколько этапов:
- Осторожная ликвидация некротических тканей из полости вручную двусторонним инструментом с рабочими частями в виде мелких ложечек с острыми краями. Это позволяет не затрагивать здоровые ткани.
- Аккуратное введение кальцифицирующей массы, в состав которой входят равные части кальция глицерофосфата, глицерина и оксида цинка. Слой массы должен тонко покрывать дно и стенки полости.
- Закрытие обработанной полости временной пломбой.
- Удаление мертвых тканей, утративших жизнеспособность вследствие некроза с помощью бора (этап проводят спустя 1, 5 месяца после установки временного пломбировочного материала).
- Обработка зачищенных тканей кальцифицирующей пастой.
- Пломбировка стеклоиономерным цементом.
При реставрации фронтальной группы зубов часть стеклоиономера удаляется через 3-4 месяца. Далее косметическое восстановление требует накладывания композитного пломбировочного материала.

Можно ли избежать возникновения
Самым действенным способом профилактики лучевого кариеса считается обеспечение защиты зубной ткани от прямого действия радиации. Например, для пациентов, проходящих лечение по поводу онкологического заболевания, изготавливают специальную каппу из свинца. Перед каждым сеансом облучения пациент должен ее надеть.
Снизить последствия ионизирующего облучения, развивающиеся в ротовой полости, помогают эндодонтические методики, а также ряд мероприятий, проводимых до лечения, в процессе и после него.
За 5 дней до лучевой терапии
Комплекс лечебно-профилактических мероприятий по оздоровлению полости рта:
- Профессиональная чистка от налета и камня.
- Лечение кариозных поражений, пульпита.
- Перепломбировка (проводится в случае наличия старых пломб).
- Лечение заболеваний десен и слизистой оболочки.
- Экстракция нежизнеспособных единиц из альвеолы.
В день первого сеанса облучения
Чтобы предотвратить вторичное облучение, перед противоопухолевой терапией, больному необходимо снять металлические протезные конструкции и пломбы из амальгамы.
Этой же цели можно достичь при помощи толстых резиновых кап (толщина не менее 3 мм), которые надевают на челюстные ряды во время процедуры облучения.
Рекомендуется часто орошать полость рта составами на базе хлорида натрия или эпинефрина. Также эффективны обработки преднизолоном.
В течение курса облучения
- Запрещено носить съемные протезные конструкции и ортодонтические аппараты.
- В пищу рекомендуется употреблять измельченные продукты с высоким содержанием белка, богатые витаминами и полезными микроэлементами.
- Гигиеническое очищение ротовой полости стоит проводить с осторожностью, избегая резких движений щеткой.
После противоопухолевой лучевой терапии
Снизить риск развития осложнений после облучения помогает местная и общая реминерализация тканей зубов.
Терапевтические мероприятия дополняются назначением средств, ведущих борьбу с окислением в клетках и радиозащитных препаратов. Наибольшую эффективность показали следующие медикаментозные продукты:
- Кальция Глицерофосфат;
- биологически активная добавка на основе экстракта морской водоросли ламинарии;
- Фитолон, обладающий выраженным иммуномодулирующим, антиоксидантным и антисептическим действием;
- витаминные комплексы.
При первых проявлениях послелучевых осложнений
При развитии негативных реакций после облучения медики рекомендуют проводить следующие профилактические мероприятия:
- Ротовые ванночки раствором чистой воды и марганцовки.
- Обработка единиц и мягких тканей полости рта антисептическими средствами низкой концентрации. Для этих целей подойдут слабые растворы фурацилина, перекиси водорода, борной кислоты.
В период сильно выраженных послелучевых проявлений
- полоскание ротовой полости низкоконцентрированными растворами антисептических средств;
- обработка слизистых оболочек цитралем в форме спиртового раствора 1%;
- снижение болевых ощущений с помощью Новокаина Дикаина или Анестезина на базе масла.
В этот период нельзя удалять зубы, выполнять глубокое очищение пародонтальных карманов и проводить другие инвазивные процедуры.
Нормализация состояния слизистых оболочек полости рта наступает через 7-8 недель после облучения.
В видео представлены некоторые факторы о современной лучевой терапии.
Отзывы
Лучевые кариозные поражения – это следствие лечения пациентов с онкологическими заболеваниями в области головы и шеи. При такой клинике разрушительные процессы в структурах зубов не первостепенная проблема.
Несмотря на это, лучевой кариес сопровождается неприятными ощущениями, снижением функциональности челюстного аппарата и эстетическими недостатками.
Если вам или вашим родственникам приходилось столкнуться с таким заболеванием, расскажите нашим читателям об эффективных способах устранения проблемы в комментариях к этой статье.
Если вы нашли ошибку, пожалуйста, выделите фрагмент текста и нажмите Ctrl+Enter.
похожие статьи
Источник

