Лечение рака предстательной железы после радикальной простатэктомии
Оперативное удаление опухоли, облучение и химиотерапия не являются 100% гарантией исцеления рака предстательной железы. Благополучный исход определяют ранее выявление онкологии и выраженность злокачественного процесса. Через 5 лет после лечения больше чем у 1/3 пациентов обнаруживается рецидив рака простаты, через 10 лет РПЖ повторно диагностируют у > 50% мужчин. Под рецидивом понимают пальпаторно определяемую опухоль, метастазы и повышение показателей ПСА.
Этиология и патогенез
Возвращение болезни после операции происходит в результате неполного удаления раковых клеток. Последующие радио- и химиотерапевтические мероприятия по разным причинам оказываются неэффективными. Формируется новая опухоль либо обнаруживаются метастазы. Рецидив рака простаты чаще развивается у пациентов, начавших борьбу с онкологией поздно, на 3–4-й стадиях болезни. В этой ситуации онкологический процесс возобновляет метастатический узел.
Различают два вида рецидива:
- Местный (локальный) – поражает только предстательную железу. Обычно наступает через 2 года после операции. Характеризуется повышением уровня ПСА в 2 раза.
- Системный – в онкологический процесс вовлекаются другие органы. Биохимический рецидив развивается быстро – ПСА за год после РПЭ увеличивается более чем в 2 раза.
Новая волна злокачественного процесса возникает в результате некорректного либо запоздалого лечения. Возобновить рак может дессеминация организма мутировавшими клетками. Основные причины рецидива.
- неполное удаление опухоли в ходе операции;
- неэффективность лучевой и химиотерапии;
- позднее начало терапии (при 3–4 степени).
Полное излечение от рака простаты возможно при первых двух стадиях при условии своевременного лечения. Риск возвращения онкологии повышает прорастание опухоли в близлежащие органы.
Симптомы и проявления
Начало заболевания проходит незаметно. Первые симптомы местного рецидива возникают по мере роста раковой опухоли и сдавливания ею мочеиспускательного канала. Возникают проблемы с мочеиспусканием, потенцией и эякуляцией. Характерные симптомы:
- ощущение наполненности мочевого пузыря;
- частые позывы, вялая струя урины;
- беспрерывные боли в паху;
- нарушение потенции, ее отсутствие;
- боли при семяизвержении;
- наличие крови в эякуляте;
- эпизодические боли внизу живота.

Задайте вопрос врачу-урологу!

Колоколов В.Н.
Запущенные стадии характеризуются разрастанием опухоли за границы капсулы железы, поражением окружающих тканей, прогрессивным метастазированием в соседние и отдаленные органы. Далее процесс распространяется на поясничный сегмент позвоночника, кости таза и конечностей. Эта стадия проявляется:
- сильными болями в позвоночнике, тазу;
- появлением неврологических расстройств;
- повышением частоты патологических переломов;
- хронической усталостью и слабостью;
- утратой аппетита, сильным похуданием.

Для инфильтрации опухоли в прямую кишку характерны проблемы с дефекацией (запоры, опорожнения с кровью). Достаточно быстро в злокачественный процесс вовлекаются легкие, печень, почки и головной мозг. Развивается последняя стадия рака, обычно с печальным финалом. Клиника системного рецидива РПЖ зависит от топографии метастазирования:
- в легких – боль в грудине, кашель, кровохаркание;
- печени – боль, увеличение печени, желтизна, отеки;
- почках – боли в пояснице, гематурия, дизурия;
- в мозге – сильные головные боли, тошнота.
Для поздних стадий рецидива рака простаты после РПЭ характерны общее истощение, кахексия с признаками интоксикации (повышение температуры тела, лихорадочное состояние).
Диагностика
После оперативного удаления опухоли и специфического лечения пациенты наблюдаются у уролога-онколога. Контролируется уровень ПСА – маркера карциномы простаты. Предположением на возвращение рака простаты будет повышение результатов выше 0,2 нг/мл. Это является поводом к обследованию. Диагностические мероприятия:
- Ректальный осмотр. Выявляет местный рецидив рака на этапе, когда опухоль разрослась и пальпируется через стенку прямой кишки.
- Опрос и осмотр пациента, выявление жалоб. Выясняется состояние больного: наличие и выраженность болей, потеря в весе.
- Биохимическое тестирование. Анализы крови (общий развернутый, на сахар, ПСА) и мочи.
- Аппаратные методы (ТРУЗИ, МРТ, КТ) – дают возможность определить рецидив на раннем этапе. Томография позволяет обнаружить метастазы.
Проводятся ПЭТ (двухфотонно-эмиссионная томография), сканирование с фтордезоксиглюкозой. Перед исследованием вводится радиофармпрепарат, маркирующий атипичные клетки.
Как проводится лечение
Тактика и длительность лечебных мероприятий рецидива рака простаты после лучевой терапии и операции отличаются и зависят от первичной методики. При недостаточной эффективности облучения назначается химиотерапевтический курс либо альтернативный метод. При местной форме эффективна дистанционная радиотерапия. Системный рак простаты лечат специфическими гормональными препаратами. Новыми эффективными методами лечения рецидива РПЖ являются следующие.
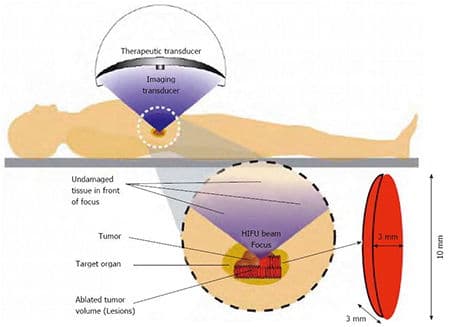
Спасительная (сальважная) HIFU терапия – при местном расположении опухоли у пациентов, перенесших полную простатэктомию. Используется высокоинтенсивный фокусированный ультразвук (High Intensity Focused Ultrasound).
Фотодинамическая терапия (ФДТ) — в/венное, локальное введение фотосенсибилизаторов, безопасных веществ, действующих на пораженный орган световым лучом заданной волны. Включает этапы:
- введение фотосенсибилизирующего препарата (минуты);
- накопление его в тканях-мишенях (дни);
- облучение опухоли лазером через световод (минуты);
- высвобождение токсинов, избирательно уничтожающих атипичные клетки.
Брахитерапия (контактное облучение) — источник излучения находится внутри ткани органа. При возобновлении рака простаты после облучения возможны локальная HIFU- и брахитерапия.
Пациент с диагнозом РПЖ после радикальной простатэктомии периодически обследуется у онколога. Проводится динамичное наблюдение показателей простатического антигена. При рецидиве рака терапевтическая тактика зависит от типа опухоли и характера ее прорастания. Учитываются возраст, иммунный статус, сопуствующие патологии. При биохимическом сигналом возвращения будет повышение уровня ПСА в крови. В этом случае назначается гормонотерапия с целью снижения уровня тестостерона.

Системный рецидив предполагает метастазирование раковых клеток в соседние органы и далее. Поздние стадии имеют выраженную онкологическую клинику. Метод борьбы со злокачественным процессом зависит от клинической ситуации. Мероприятия: химиотерапия, облучение, операция, гормональная терапия, фокусированная УЗ-абляция. Лекарства, назначаемые врачом при раке простаты:
- Золадекс (Гозарлин)— аналог гонадотропин-рилизинг гормона, назначается при гормон-резистентной форме патологии. Снижает уровень ПСА.
- Андрокур (ципротерона ацетат) — антиандроген, кастрационный препарат, осуществляет полную гормональную блокаду. Показания — метастазирующий и неоперабельный рак.
- Флутамид — нестероидный антиандроген. Препятствует усвоению клетками мужских гормонов. Снижает уровень тестостерона и, как следствие, ПСА.
Суть терапии биохимического рецидива РПЖ — нормализация показателей ПСА. Клинические рекомендации при малоэффективности гормональной терапии склоняются к проведению орхиэктомии (удалению тестикул).
Прогноз
Выживаемость пациентов с раком простаты довольно высокая. В среднем 80—90% своевременно оперированных остаются живы через 5 лет. Рецидивы также достаточно часты, 15—30% больным не удается одолеть онкологию. Смертность в течение 10 лет составляет 15—20 %. На статистику выживаемости влияет исходный уровень ПСА: чем меньше его показатели после радикальной простатоэктомии, тем лучше прогноз.
Выраженность распространения злокачественного процесса дает возможность оценить исход заболевания. Важным прогностическим фактором после РПЭ является положительный хирургический край. Рост новообразования по краю резекции и его выход за пределы капсулы значительно сокращают выздоровление.
В течение 5 лет у оперированных пациентов с негативным хирургическим краем вероятность рецидива — всего 20%, с позитивным — 40—60%. При прорастании опухоли в семенные пузырьки после удаления простаты местный рецидив рака возникает в 70% случаев. Хорошая 10-летняя выживаемость отмечается после брахитерапии (86%).
Вы нашли то, что искали?
Если у вас остались вопросы, задайте их в комментариях (это абсолютно анонимно и бесплатно). По возможности, я или другие посетители сайта помогут вам.
Источник
Радикальная простатэктомия (РПЭ) — самый эффективный метод лечения локализированных форм рака, который позволяет полностью удалить опухоль. Однако даже удаление первичного очага заболевания не исключает появления отдаленных метастазов в послеоперационный период. По имеющимся данным, в России в течение 10 лет после проведения операции у 35 — 40% пациентов с клинически локализованным раком простаты возникает рецидив, при этом у 95% он диагностируется в первые 5 лет после операции.
Причины рецидива рака простаты
Основная причина рецидива рака простаты после радикальной простатэктомии — оставшиеся в организме пораженные клетки, которые в активном состоянии способны к неконтролируемому размножению.
Как в организме остаются злокачественные клетки? В первую очередь, это отдалённые вторичные очаги — метастазы, которые в момент проведения оперативного вмешательства присутствуют в организме. Они распространяются как в ткани ближайших органов (семенные пузырьки, тазовые лимфоузлы, шейку мочевого пузыря, кишечник), так и в печень, легкие, кости осевого скелета, органы центральной нервной системы. Рецидив такого вида называют метастатическим.
После операции по удалению простаты может возникнуть локальный рецидив — при образовании позитивного хирургического края, который представляет собой неиссеченные раковые клетки, оставшиеся после удаления опухоли. Позитивный хирургический край может образоваться, когда рак распространяется за капсулу предстательной железы или при низком качестве оперативного вмешательства.
Факторы прогноза местного рецидива рака простаты после РПЭ
Прогрессирование рака простаты после радикальной простатэктомии происходит крайне медленно и практически бессимптомно. Риск развития рецидива определяют по совокупности биомаркеров: уровню сывороточного ПСА, плотности ПСА патологоанатомической стадии рака, сумме Глисона, характеру хирургического края, объему удаленной опухоли, лимфоваскулярной и периневральной инвазии. Общепризнанным фактором прогноза рецидива также является предоперационный уровень ПСА в сочетании со степенью распространенности рака.
Уровень простатспецифического антигена
Исследования C.R. Pound в 1999 году показали, что все без исключения случаи рецидива рака простаты сопровождаются повышением уровня простатического специфического антигена (ПСА) — протеина, вырабатываемого клетками предстательной железы. В течение 2-3 недель сразу после успешного проведения радикальной простатэктомии у подавляющего большинства пациентов уровень ПСА снижается до пороговых значений.
Любой рост уровня антигена и его отличная от нуля величина могут быть индикатором локального или отдаленного рецидива рака. Поэтому оценку уровня рекомендуется проводить через 3 и 6 месяцев после операции, затем в течение первых трех лет после РПЭ — через каждые полгода, в дальнейшем — 1 раз год.
Однако если после удаления опухоли остался позитивный хирургический край, уровень ПСА также может незначительно повышаться, при этом другие клинические признаки опухолевого процесса отсутствуют.
На сегодняшний день пороговым значением неблагоприятного прогноза, которое может свидетельствовать о наступлении рецидива рака простаты после радикальной простатэктомии, считается повышение ПСА до 0,2 нг/мл и более в двух последовательных измерениях. При этом вероятность прогрессирования болезни увеличивается, если скорость роста уровня антигена превышает в год 0,75 нг/мл, а удвоение ПСА наступает за срок менее 10 месяцев. При этом также принимают во внимание плотность ПСА — отношение дооперационного уровня антигена к объему удаленной простаты.
Сумма Глисона
Злокачественные опухоли простаты неоднородны. Для оценки структурной дифференцировки злокачественного образования используется сумма Глисона. Она определяется в результате сложения приведенных к пятибалльной шкале результатов гистологического исследования двух участков пораженной железы и позволяет оценить степень прогрессирования опухоли. Минимальный риск развития рецидива у пациентов с локализованной формой рака при показателе Глисона 6, максимальный — при значении от 8 до 10.
Характер хирургического края
При «чистых» краях резекции прогноз развития рецидива минимален, он составляет не более 16%. В то время как при позитивном хирургическом крае — 26%. Уменьшить риск образования позитивного хирургического края позволяет радикальная робот-ассистированная простатэктомия Да Винчи. Система роботической хирургии предоставляет хирургу 3D-изображение и 20-кратное увеличение оперируемой области, что позволяет полностью удалить пораженные ткани.
Совокупность вышеперечисленных факторов, а также объем удаленной опухоли более 4 куб. см, лимфоваскулярная и периневральная инвазия и стадия рака от Т2а и выше увеличивают риск возникновения местного рецидива рака простаты после радикальной простатэктомии.
Диагностические исследования
При возрастании уровня ПСА после РПЭ для уточнения диагноза на ранних стадиях развития рецидива используют современные методы визуализации.
- Трансректальное УЗИ (при подозрении на локальный рецидив и как метод контроля при проведении биопсии).
- Эндоректальная МРТ малого таза с контрастным усилением (идентифицирует рецидивирующие опухоли при относительно низких значениях ПСА).
- Мультиспиральная компьютерная томография (выявление висцеральных и костных метастазов, оценка состояния лимфоузлов).
Проведение компьютерной и магнитно-резонансной томографии рекомендуется пациентам с повышенным уровнем сывороточного ПСА, а также при жалобах на боли в костях (независимо от уровня ПСА).
Методы лечения рецидива
Локализованная форма
Пациентам с высоким риском рецидива может быть рекомендовано проведение адъювантной лучевой терапии сразу после операции. Облучению подвергают ложе удаленной предстательной железы и регионарные лимфатические узлы. Полный курс лечения длится около 7 недель, сессии облучения — ежедневно.
Метастатический рецидив
На стадии рака T3a-bN0/1M0 после РПЭ при низкой распространенности процесса для предотвращения рецидива рекомендовано применение лучевой терапии в комбинации с курсом андрогенной депривации. Пациентам с тяжелыми сопутствующими заболеваниями может быть назначена гормональная терапия или комбинация гормональной и химиотерапии.
Выбор метода лечения для каждого пациента определяется индивидуально в зависимости от стадии заболевания, группы риска, размера опухоли, значений биомаркеров.
Источник
Рак предстательной железы (РПЖ) диагностируют у 32 – 40% мужчин старше 50 лет. В половине случаев это локализованный рак, то есть опухоль не выходит за пределы простаты. Стандартом лечения в такой ситуации считается радикальная простатэктомия – одномоментное удаление новообразования. Не уступает по радикальности и лучевая терапия, которую часто рассматривают как альтернативу операции. Тем не менее, лечение не всегда эффективно. Иногда болезнь возвращается спустя несколько месяцев или лет после радикального лечения. Такое состояние называется рецидивом рака предстательной железы, который может быть локальным или местным, системным и биохимическим.
Вероятность рецидива после радикальной простатэктомии составляет от 10 до 28% в первые 5 лет после вмешательства. Это зависит от строения опухоли, соматического состояния пациента, размера новообразования. Например, если радикальную простатэктомию выполняли на стадии T3а (рак распространяется на клетчатку вокруг простаты), вероятность возрастает до 45%.

Развитие рецидива в течение 5 лет после лучевой терапии составляет 12 – 38%. При этом будут иметь значение не только особенности новообразования, но и доза облучения – чем она меньше, тем выше риски. Вид воздействия (брахитерапия или дистанционное) большой роли не играет.
Если же говорить о сроках в целом, 45% случаев регистрируются в течение 2 лет после радикального лечения, 77% – в пределах 5 лет, 96% – на протяжении 9 лет.
Биохимический рецидив
Протекает бессимптомно и определяется исключительно по результатам анализа на уровень простатспецифического антигена (ПСА или PSA). Это особый белок, который есть только в тканях предстательной железы. Соответственно, после ее удаления, уровень простатспецифического антигена должен резко снизиться до значений, не определяемых стандартными методами исследований. Если же, спустя некоторое время, уровень ПСА начинает вновь возрастать, это может означать лишь то, что в организме остались клетки опухоли, которые начали размножаться. Биохимический рецидив после радикальной простатэктомии диагностируют, когда уровень ПСА систематически увеличивается через три измерения подряд на 0,2 нг/мл и более, интервал между исследованиями больше или равен 2 неделям.
Подобная ситуация возможна и после радиотерапии. Конечно, при облучении часть тканей железы остается жизнеспособной и уровень ПСА не опускается до неопределяемых значений. Поэтому за исходную точку берут самый низкий уровень антигена.
Критерием биохимического рецидива считается повышение показателя PSA более чем на 2 нг/мл по сравнению с минимальным значением, отмечавшимся у больного.
Биохимический рецидив рака предстательной железы лечат облучением ложа простаты, иногда вместе с захватом области регионарных лимфоузлов.
Локальный рецидив
Локальный рецидив рака простаты после радикальной простатэктомии регистрируется в 15 – 35% случаев. Местным — считается появление очага опухоли в области расположения удаленной предстательной железы при отсутствии поражения лимфоузлов и отдаленных метастазов. Этот очаг должен быть визуализирован, то есть виден на УЗИ, компьютерной томограмме, при МРТ-обследовании или ПЭТ — КТ. Его злокачественность должна подтверждаться гистологически – то есть после взятия биопсии и исследования под микроскопом.
Клинических симптомов на ранней стадии обычно не бывает. Чаще всего во время очередного профилактического обследования у пациента обнаруживают вновь повысившийся уровень ПСА, после чего проводят углубленную диагностику и выявляют местный рост опухоли. Если пациент, вопреки рекомендациям, не обследуется профилактически после радикального лечения и рецидив на ранних стадиях не выявлен, на поздних этапах развития возвращаются некоторые симптомы запущенных стадий рака простаты: боли в промежности и над лобком, задержка мочи, запоры.

Локальный рецидив, визуализированный при помощи ПЭТ — КТ у пациента с повышенным уровнем PSA после РПЭ
Лечение локального рецидива РПЖ зависит от того, какой метод был использован ранее.
Если первично возникший рак лечили с помощью лучевой терапии, при рецидиве выполняют радикальную простатэктомию (РПЭ). При этом вероятность послеоперационных осложнений выше, чем если бы хирургическое вмешательство было сделано при первичном раке: после облучения возрастает опасность повреждения прямой кишки, увеличивается кровопотеря во время вмешательства, высок риск возникновения недержания мочи, или, наоборот, контрактуры (патологического сокращения) шейки мочевого пузыря. 5-летняя безрецидивная выживаемость после операции 55 – 69%.
Если же первично была выполнена РПЭ, при лечении рецидива рака используют лучевую терапию. 5-летняя безрецидивная выживаемость при этом зависит от исходного уровня ПСА. Если он меньше 0,2 нг/мл, показатель 5-летней безрецидивной выживаемости достигает 77%, при 0,2 нг/мл опускается до 34%, а если уровень ПСА доходит до 1 нг/мл, прогноз расценивается как неблагоприятный.
Из экспериментальных методов, достоверной статистики эффективности которых пока нет, применяется криоабляция (замораживание) и воздействие сфокусированным ультразвуком высокой интенсивности (HIFU-терапия). Несмотря на то, что предварительные результаты исследований эффективности методик довольно обнадеживающие, в официальные гайдлайны эти манипуляции пока не включены.
Системный рецидив
Случается и так, что на момент радикального лечения остались недиагностированные микрометастазы, которые продолжили свое развитие после вмешательства. В этом случае трудно отличить системный рецидив (возобновление роста новообразования) от системной прогрессии опухоли (продолжения развития не удаленных очагов).
Отчасти, их можно различить по следующим критериям:
- повышение концентрации ПСА менее чем через год после операции;
- уровень ПСА удваивается за 4 – 6 месяцев;
- 8 – 10 баллов по шкале Глисона.
Системный рецидив клинически проявляется такими же симптомами, как и метастатический рак. Поскольку злокачественные новообразования предстательной железы метастазируют в кости, легкие, печень, возникают признаки поражения этих органов:
- боли в костях;
- патологические переломы;
- повышенный уровень кальция и щелочной фосфатазы крови;
- боли в позвоночнике;
- парезы, параличи (при сдавлении спинного мозга);
- боли в подреберье;
- увеличение печени;
- анемия.
Эти проявления сопровождаются общим недомоганием, повышением температуры до 37-38, потерей аппетита, резким снижением массы тела.
При системном рецидиве, равно как и при прогрессии рака предстательной железы применяют гормонотерапию, чаще всего – кастрацию.
Метастазы в кости подвергаются радиотерапии – облучение помогает уменьшить интенсивность болевого синдрома.
Прогноз сомнительный.
Источник

