Лечение нарушений внешней секреции поджелудочной железы
Поджелудочная железа – многофункционный орган системы пищеварения. Можно сказать, что она предстает главным органом пищеварения, принимает участие в процессах обмена в организме человека.
Обладает диффузным функционалом – внешний и внутренний. Внешнесекреторная задача обусловлена выработкой панкреатического сока, который включает в себя ферменты пищеварения, нужные для нормального переваривания пищи.
Внутрисекреторный (эндокринный) функционал заключается в продуцировании определенных гормональных составляющих, обеспечивает регуляцию процессов обмена – жировой, углеводный и белковый обмен.
Расстройство функциональности поджелудочной железы провоцирует возникновение патологий – сахарный диабет, панкреатит и др. Рассмотрим анатомию и физиологию внутреннего органа, что позволит лучше узнать собственный организм.
Расположение и строение поджелудочной железы
ПЖ локализуется в брюшной области, находится сзади желудка, вплотную прилегает к 12-перстной кишке на уровне верхних позвонков поясницы. В проекции на брюшную стенку она располагается на 5-10 сантиметров выше пупка. Орган характеризуется трубчатым строением, состоит из трех сегментов – головка, тело и хвост.
Головка органа размещается в области изгиба 12-перстной кишки, последний орган охватывает головку в виде подковы. От тела она отделяется бороздой, по которой происходит воротная вена внутри организма.
Снабжение железы кровью происходит через артерии, отток биологической жидкости осуществляется посредством воротниковой вены.
Особенности строения тела ПЖ:
- Тело подразделяется на несколько частей – передняя, нижняя и задняя части, аналогично выделяют края.
- Передняя часть соприкасается со стенками желудка.
- Задняя часть примыкает к брюшной аорте и позвоночнику, по ней проходят кровеносные сосуды селезенки.
- Нижняя часть располагается пониже корня поперечной ободочной кишки.
Хвост ПЖ доходит до ворот селезенки, направлен и вверх и вниз. Структура внутреннего органа состоит из двух типов ткани, которые выполняют внешнюю и внутреннюю функцию. Основа ткани – мелкие дольки, которые разделяются между собой посредством прослоек соединительной ткани.
У каждой дольки имеются свои протоки на вывод. Они соединяются между собой, вследствие чего образуется общий выводной проток, который проходит по всему органу. У правого края головки он открывается в 12-перстную кишку, соединяется с желчными протоками. Вот так секрет поджелудочной железы проникает в кишку.
Между дольками локализуются группы клеток, называемые островками Лангерганса. Они не имеют выводных протоков, однако обладают сетью сосудов крови, что позволяет выделять инсулин и глюкагон сразу в кровь.
Как регулируется работа железы?
Уровень сахара
Мужчина
Женщина
Укажите Ваш сахар или выберите пол для получения рекомендаций
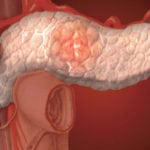 Регуляция панкреатической секреции предстает многоуровневым процессом. Большое влияние на активность функциональности клеток, которые способны секретировать нужные ферменты, оказывает состояние центральной нервной системы.
Регуляция панкреатической секреции предстает многоуровневым процессом. Большое влияние на активность функциональности клеток, которые способны секретировать нужные ферменты, оказывает состояние центральной нервной системы.
Исследования показывают, что вид пищи, запах еды или просто упоминание о ней приводят к резкому увеличению активности ПЖ. Это воздействие базируется на работе вегетативного отдела нервной системы.
Парасимпатический отдел нервной системы посредством блуждающего нерва способствует повышению активности внутреннего органа. При этом симпатическая система ориентирована на снижение.
В регуляции деятельности органа большое значение придается свойствам желудочного сока. Если увеличивается кислотность его в желудке, наблюдается его механическое растяжение, это приводит к тому, что возрастает секреция поджелудочной железы.
Одновременно с этим механическое растяжение 12-перстной кишки и увеличение кислотности в ее просвете приводит к выработке веществ, которые стимулируют работу ПЖ. К этим веществам относят:
- Секретин.
- Холецистокинин.
Железу системы в организме могут не только стимулировать, но и тормозить ее работу. Это влияние оказывается под воздействием симпатической нервной системы и гормонов – глюкагон, соматостатин.
Железа может подстраиваться под ежедневное меню. Если в еде превалируют углеводы, то синтезируемый секрет содержит преимущественно амилазу; если в пище больше белковых веществ, то вырабатывается трипсин; на фоне потребления только жирных продуктов питания продуцируется липаза.
Функции органа пищеварительной системы
Внешнесекреторная деятельность поджелудочной железы подразумевает выработку панкреатического сока. В сутки она синтезирует 500-1000 мл оного. Он состоит из ферментных соединений, соли и обычной воды.
Ферменты, которые синтезируются посредством железы, называют проферменты. Они продуцируются в неактивной форме. Когда попадает еда в 12-перстную кишку, начинают выделяться гормоны, посредством которых запускаются биохимические цепочки в организме, что приводит к активизации ферментов.
Мощным стимулятором выступает соляная кислота, которая при попадании в кишку способствует выведению секретина и панкреозимина – они оказывают воздействие на синтезирование ферментов:
- Амилаза обеспечивает расщепление углеводов.
- Трипсин принимает участие в процессе переваривания белковых веществ, который берет свое начало в желудке.
- Липаза помогает расщеплять жиры, которые уже подверглись влиянию желчи, поступившей из желчного пузыря.
Также панкреатический сок включает в свой состав минеральные вещества в виде кислой соли, которые способствуют щелочной реакции. Это нужно для того чтобы нивелировать кислые составляющие продуктов питания, которые поступили из желудка, и создать благоприятную среду для усвоения углеводов.
Внутрисекреторная функция органа обеспечивает выделение в организм таких гормонов как инсулин и глюкагон. Они продуцируются посредством группы клеток, которые вкраплены между дольками, не обладают протоками – островками Лангерганса. Функции гормонов:
- Выделение инсулина наблюдается из бета-клеток. Этот гормон отвечает за регулирование углеводных и жировых процессов в организме. Под воздействием компонента глюкоза проникает в ткань и клетки, вследствие чего концентрация сахара снижается.
- Глюкагон продуцируется посредством альфа-клеток. Если кратко, то гормон – это антагонист инсулина, то есть, ориентирован на повышение содержания сахара в организме человека. Также альфа-клетки участвуют в синтезировании липокаина, который предупреждает жировое перерождение печени.
Выделение адреналина из надпочечников также регулируется концентрацией сахара. На фоне гипогликемического состояния (низкая глюкоза) наблюдается рефлекторная выработка адреналина, что способствует повышению содержания сахара.
Поджелудочная железа находится в тесной связи с остальными органами пищеварительной системы. Любые ее нарушения или сбои в работе пагубным образом отражаются на всем процессе пищеварения.
Клинические проявления дефицита ферментов ПЖ
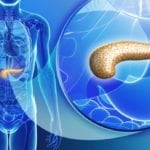
Расстройство выработки ферментов, снижение их функциональности и дефицит – это последствия хронической формы панкреатита. Заболевание сопровождается постепенными изменениями железистой ткани, вследствие чего она замещается соединительной тканью.
К панкреатиту приводит множество причин. Однако чаще всего патологический процесс в организме обусловлен чрезмерным потреблением алкогольных напитков. Среди другой этиологии выделяют нерациональное питание, сопутствующие недуги (холецистит), инфекционные заболевания, прием некоторых лекарственных средств.
Дефицит трипсина, амилазы и липазы приводит к серьезным сбоям в работе пищеварительного процесса.
Общие симптомы сбоя в работе ПЖ:
- Болевой синдром в левой области живота в подреберье, который часто развивается после приема пищи. Иногда боли не связаны с едой.
- Понижение или полная потеря аппетита.
- Пищеварительные расстройства в виде тошноты, поноса, многократной рвоты.
- Урчание в животе, метеоризм.
- Изменяется окраска и консистенция кала.
Выраженность и интенсивность клинических проявлений обусловлены степенью поражения. Из-за плохого переваривания наблюдается дефицит питательных компонентов, а в некоторых картинах расстройства метаболических процессов приводит к др. патологиям – остеохондроз, остеоартроз, атеросклероз кровеносных сосудов.
Если выявляется нехватка именно липазы, то признаки следующие:
- В каловых массах присутствует избыточное наличие жира.
- Жидкий кал оранжевого либо желтого цвета.
- Стул маслянистый.
В некоторых случаях происходит выделение только жидкого жира без наличия каловых масс. Если не хватает амилазы, то у больного обнаруживается непереносимость еды, обогащенной моносахаридами и дисахаридами. Также присутствует жидкий стол, недостаточность всасывания компонентов в тонком кишечнике, что сопровождается постоянным поносом, понижением массы тела.
При дефиците трипсина просматривается умеренная либо выраженная креаторея – в фекалиях выявляется большое содержание азота и мышечных волокон. Стул характеризуется зловонным запахом, не исключается возникновение малокровия.
Поскольку механизм расщепления продуктов нарушен, то даже при усиленном питании у пациентов понижается вес, диагностируется дефицит витаминов и минеральных компонентов, чрезмерная сухость кожного покрова, ломкость ногтевых пластин, волос.
При низкой выработке ферментов железой рекомендуется заместительное лечение. Но вещества растительной природы не могут полностью компенсировать внешнесекреторную недостаточность органа.
Как лечат железу?
 Лечение обусловлено конкретным заболеваниям. Острый приступ на фоне уточненных и неуточненных причин лечится посредством голодания. Поскольку это помогает снизить продуцирование сока, как результат, разгружается внутренний орган.
Лечение обусловлено конкретным заболеваниям. Острый приступ на фоне уточненных и неуточненных причин лечится посредством голодания. Поскольку это помогает снизить продуцирование сока, как результат, разгружается внутренний орган.
Обычно голодание при панкреатите пациенты легко переносят, так как значительно ухудшается общее самочувствие, присутствует постоянный болевой синдром. Разрешается пить минеральную воду без газа либо слабоконцентрированный отвар шиповника.
Основная цель терапии острого заболевания – предупредить осложнения и его перерождение в вялотекущий процесс. Рекомендуются таблетки для снятия болевого синдрома и ферментативные лекарства, которые способствуют снижению секреции ферментов.
Изначально они вводятся в организм человека через вену. Когда у пациента выявляется улучшение самочувствия, то он уже может принимать медикаменты в виде таблеток. Чтобы снизить болезненные ощущения в острой фазе можно к ПЖ прикладывать грелку со льдом.
Препараты для терапии поджелудочной железы:
- Спазмолитики для снятия болевого синдрома. Медицинские специалисты в большинстве назначают Папаверин, Но-шпу, Дротаверин. Если боль умеренная, то применяют Ибупрофен. Последнее лекарство одновременно обладает противовоспалительным и обезболивающим свойством.
- Антацидные медикаменты помогают унять боль, предупреждают раздражение и изъязвление слизистой оболочки. Используют в виде растворов и гелей, которые помогают нейтрализовать соляную кислоту. Представители группы – Зоран, Ранитидин.
Чтобы снизить выработку пищеварительных ферментов применяют Контрикал. Для терапии хронического панкреатита нужно ферментное лечение, чтобы поддерживать работу внутреннего органа, улучшить процесс переваривания пищи. Назначают Мезим, Панкреатин, Креон.
Поджелудочная железа является очень нежным и чувствительным органом, поэтому требует бережного отношения к себе. Злоупотребление алкоголем и вредные пищевые привычки могут привести к панкреатиту – острому и хроническому заболеванию, камням в выводных протоках, сахарному диабету, некрозу либо аденокарциноме ПЖ и др. заболеваниям.
Строение и функции поджелудочной железы рассмотрены в видео в этой статье.
Уровень сахара
Мужчина
Женщина
Укажите Ваш сахар или выберите пол для получения рекомендаций
Последние обсуждения:
Источник
Объем
секрета поджелудочной железы составляет
1500 мл в сутки. Он выделяется в тонкую
кишку и содержит ферменты, гидролизирующие
белки, жиры и углеводы. Регуляция секреции
осуществляется гормонами — холецистокинином
(стимулирует секрецию ферментов) и
секретином (стимулирует секрецию
бикарбонатов). Регуляция панкреатической
секреции осуществляется через блуждающий
нерв.
Основными
причинами нарушений внешней секреции
поджелудочной железы являются: 1)
недостаточная продукция секретина при
ахлоргидрии; 2) неврогенное торможение
функции поджелудочной железы (при
ваготомии, отравлении атропином); 3)
развитие аллергических реакций; 4)
воздействие различными химическими
веществами (отравление фосфором, свинцом,
ртутью, кобальтом); 5) травмы брюшной
полости; 6) токсикоинфекции (брюшной
тиф, паратифы); 7) хронические инфекции
(туберкулез, малярия); 8) алиментарные
факторы (избыточный прием пищи, животных
жиров и др.); 9) разрушение поджелудочной
железы опухолевым процессом; 10) закупорка
и сдавление протока опухолью; 11) дуо-
дениты
— воспалительные процессы в ДПК любой
этиологии (инфекционные, паразитарные
и др.), ведущие к уменьшению образования
секретина, с последующей гипосекрецией
поджелудочной железы; 12) воздействие
алкоголем, усиливающим выброс соляной
кислоты, что ведет к стимуляции выработки
секретина с избыточным выделением
панкреатического секрета; 13) острые и
хронические панкреатиты.
Этиология
и патогенез острого панкреатита.
Основными
этиологическими
факторами (в
70% случаев) острого
панкреатита являются желчекаменная
болезнь и прием алкоголя. Возникновение
острых алкогольных панкреатитов
объясняется не только токсическим
воздействием алкоголя. Алкоголь
стимулирует выброс соляной кислоты,
которая, воздействуя на слизистую
двенадцатиперстной кишки, усиливает
секрецию секретина. Последний является
мощным стимулятором панкреатической
секреции, избыточное выделение которой
ведет к повышению давления в протоках
железы и развитию острого панкреатита.
Кроме того, крепкие алкогольные напитки
способствуют отеку слизистой ДПК, что
вызывает спазм фатерова соска с
последующим повышением давления в
панкреатических протоках. Известно и
непосредственное воздействие алкоголя
на сосуды поджелудочной железы, вызывающее
их спазм. Это ведет к ишемии органа с
гибелью ацинозных клеток и к активации
ферментов в ткани железы. Прием алкоголя
в дозе, превышающей 100 г/сут в течение
нескольких лет, может привести к
преципитации панкреатических ферментов
в мелких протоках и формированию белковых
пробок. Более редкими причинами развития
острого панкреатита являются травмы
живота, гиперлипидемия (особенно I и IV
типа), прием некоторых лекарственных
препаратов (азотиаприн, сульфазалазин,
фуросемид, кортикостероиды, эстрогены),
инфекции (эпидемический паротит, болезнь
Боткина, сальмонеллез), оперативные
вмешательства, диагностическая
ретроградная холангиопанкреатография,
анатомические аномалии панкреатического
протока (стриктуры, опухоли), гиперкальциемия,
уремия, сосудистые поражения, наследственная
предрасположенность.
Рассматриваются
3 механизма развития острого панкреатита.
Наиболее принята теория
самопереваривания ткани железы, согласно
которой протеолитические ферменты —
трипсиноген, химотрипсиноген, проэластаза
и фосфолипаза А активируются внутри
протока поджелудочной железы. Полагают,
что некоторые факто-
ры
(эндо- и экзотоксины, в частности алкоголь,
вирусные инфекции, ишемия и травма)
активируют проферменты, т.е. в условиях
патологии трипсиноген может активироваться
в железе под влиянием кофермента
цитокиназы, выделяющейся из поврежденных
клеток паренхимы. Важную роль в развитии
панкреатита играет и ингибитор трипсин,
который в норме в достаточном количестве
содержится в поджелудочной железе и
препятствует превращению трипсиногена
в трипсин. При большой активности
трипсина ингибиторы антиферментной
системы истощаются, и возникает их
дефицит. Это используется как тест в
диагностике острого панкреатита: чем
выше содержание трипсиногена в сыворотке
крови, тем меньше ингибитора трипсина.
При дефиците этого фактора отмечается
активный переход трипсиногена в трипсин.
Усиленная активность протеолитических
ферментов, особенно трипсина, приводит
к перевариванию ткани поджелудочной
железы и к активации других ферментов
— эластазы и фосфолипазы. Происходит
переваривание активными ферментами
клеточных мембран, развивается протеолиз,
отек, интерстициальное воспаление,
повреждение сосудов, коагуляционный,
жировой некроз (стеатонекроз)
и
некроз паренхимы железы. Повреждение
и разрушение клеток ведут к высвобождению
активированных ферментов. Переваривающее
действие ферментов сказывается и на
периферии. С этим связан феномен
«уклонения ферментов в кровь», вызывающий
развитие некротических процессов в
других органах. При попадании липазы в
кровь возможны некрозы отдаленных
органов с тяжелой последующей
интоксикацией. Процесс может осложниться
перитонитом и абсцессами брюшной
полости. Трипсин активирует панкреатический
калликреин, вызывающий образование
каллидина и брадикинина, которые
усиливают повреждение ткани железы.
Идет дальнейшая активация кининовой
системы. Активация и высвобождение
брадикинина и гистамина вызывают
различные гемодинамические расстройства.
Расширяются сосуды, повышается
проницаемость их стенок и развивается
отек железы. Выход жидкости и белка в
ткани ведет к снижению онкотического
давления и развитию панкреатического
коллапса, иногда
со смертельным исходом. Этот коллапс
можно воспроизвести в эксперименте при
внутривенном введении животному
панкреатического сока. Если сок
предварительно прокипятить, то коллапс
не разовьется.
Вторая
теория — это
теория «общего канала». Благодаря
анатомической особенности у большинства
людей (у 80%) имеется об-
щий
желчный и панкреатический проток, что
облегчает рефлюкс желчи в проток
поджелудочной железы. Однако в норме
давление в панкреатическом протоке в
2 раза выше, чем в общем желчном протоке
(200 мм вод. ст.). Это предохраняет от
заброса желчи и кишечного содержимого
в протоки поджелудочной железы. Заброс
желчи может отмечаться при гипертонусе
сфинктера Одди или гипермоторной
дискинезии желчных путей. Частое развитие
панкреатита при желчекаменной болезни
объясняется происходящим повышением
давления в желчевыводящей системе. Это
обеспечивает заброс инфицированной
желчи под большим давлением в
панкреатический проток, что вызывает
химическое повреждение ткани железы,
повышает ее ферментативную активность.
Фосфолипаза желчи активирует трипсиноген.
При желчекаменной болезни приступы
острого панкреатита могут быть связаны
с преходящей обтурацией фатерова соска
желчными камнями. Заброс кишечного
содержимого возможен при зиянии фатерова
соска или при гипертонической дискинезии
ДПК, возникающей при воспалении,
воздействии алиментарных и других
факторов. При этом попадающая в железу
энтеропептидаза активирует трипсиноген.
Образовавшийся трипсин оказывает
аутокаталитическое действие — активирует
трипсиноген и другие протеолитические
ферменты. Так, если в эксперименте ввести
в проток поджелудочной железы небольшое
количество трипсина, то происходит
выраженный некроз ее ткани, поскольку
образуются активные протеолитические
ферменты.
Третья
теория объясняет развитие панкреатита
обструкцией
панкреатического протока и
гиперсекрецией.
Обструкция
(спазм сфинктера Одди, отек ДПК и др.)
вызывает задержку выделения панкреатического
секрета с последующей активацией
ферментов внутри железы.
При
панкреатите развиваются 3 стадии: острый
приступ (отек, возможно панкреонекроз),
стадия неполного излечения с персистирующим
хроническим воспалением или деструкцией
панкреатического протока и затем стадия
хронического воспаления с экзокринной
недостаточностью поджелудочной железы.
С развитием фиброзных изменений в ткани
железы, связанных с перенесенным острым
панкреатитом, наступает внешнесекреторная
(экзокринная) недостаточность поджелудочной
железы, характерная для хронического
панкреатита. В железе уменьшается, а
затем полностью прекращается (при
склерозировании, сморщивании органа)
об-
разование
пищеварительных ферментов (панкреатическая
ахилия). Нарушаются
полостное пищеварение (в полости тонкой
кишки) и всасывание. В первую очередь
резко страдает переваривание и всасывание
жиров. Жиры до 60-80% не усваиваются и в
повышенном количестве выводятся с калом
(стеаторея — выделение с калом более 5 г
в сутки или более 5-6% от введенного
изотопа — триолеат-глицерина J131).
Отмечается полифекалия, при копрологическом
исследовании в кале много нейтрального
жира (так как нарушается расщепление
жиров до жирных кислот). Стеаторея
вызывает потерю организмом кальция,
который экскретируется вместе с жирами
в виде нерастворимых мыл (в кале, кроме
нейтрального жира, будут мыла). Наряду
с ионами кальция теряются и ионы магния,
цинка, которые также образуют мыла с
невсосавшимися жирами. Развиваются
синдромы гипокальциемии, гипомагниемии.
В меньшей степени и позднее нарушается
переваривание белка (не усваивается до
30-40%). Об этом свидетельствует появление
большого количества мышечных волокон
в кале (креаторея),
особенно
после приема мясной пищи. Переваривание
углеводов также нарушается. Отмечается
снижение объема секреции поджелудочной
железы, гидрокарбонатов в панкреатическом
соке (после стимуляции секретином 1
мг/кг массы) и ферментов — амилазы,
трипсина, липазы (после стимуляции
панкреозимином 1,5 мг/кг массы). Расстройство
пищеварения усугубляется диспепсическим
симптомокомплексом. Возникает синдром
диареи, развивается синдром малдигестии,
идет прогрессирующая потеря массы тела
(в случае отсутствия заместительной
терапии).
Соседние файлы в папке Патофизиология
- #
24.03.20164.8 Mб75Адо Патологическая физиология.djvu
- #
- #
- #
- #
- #
Источник

