Лечение локализованного рака предстательной железы
Локализованный рак предстательной железы относится к опухоли, которая ограничена предстательной железой и не распространяется за ее пределы. Это может быть опухоль T1 или T2, в зависимости от ее размера и расположения в предстательной железе.
T1 означает, что опухоль слишком мала, чтобы ее можно было почувствовать во время пальцевого ректального исследования или. Опухоли стадии Т1 подтверждаются биопсией.
Опухоль T2 означает, что рак предстательной железы уже можно обнаружить при пальцевом ректальном исследовании, но по-прежнему ограничен предстательной железой. (рис.1 и 2). 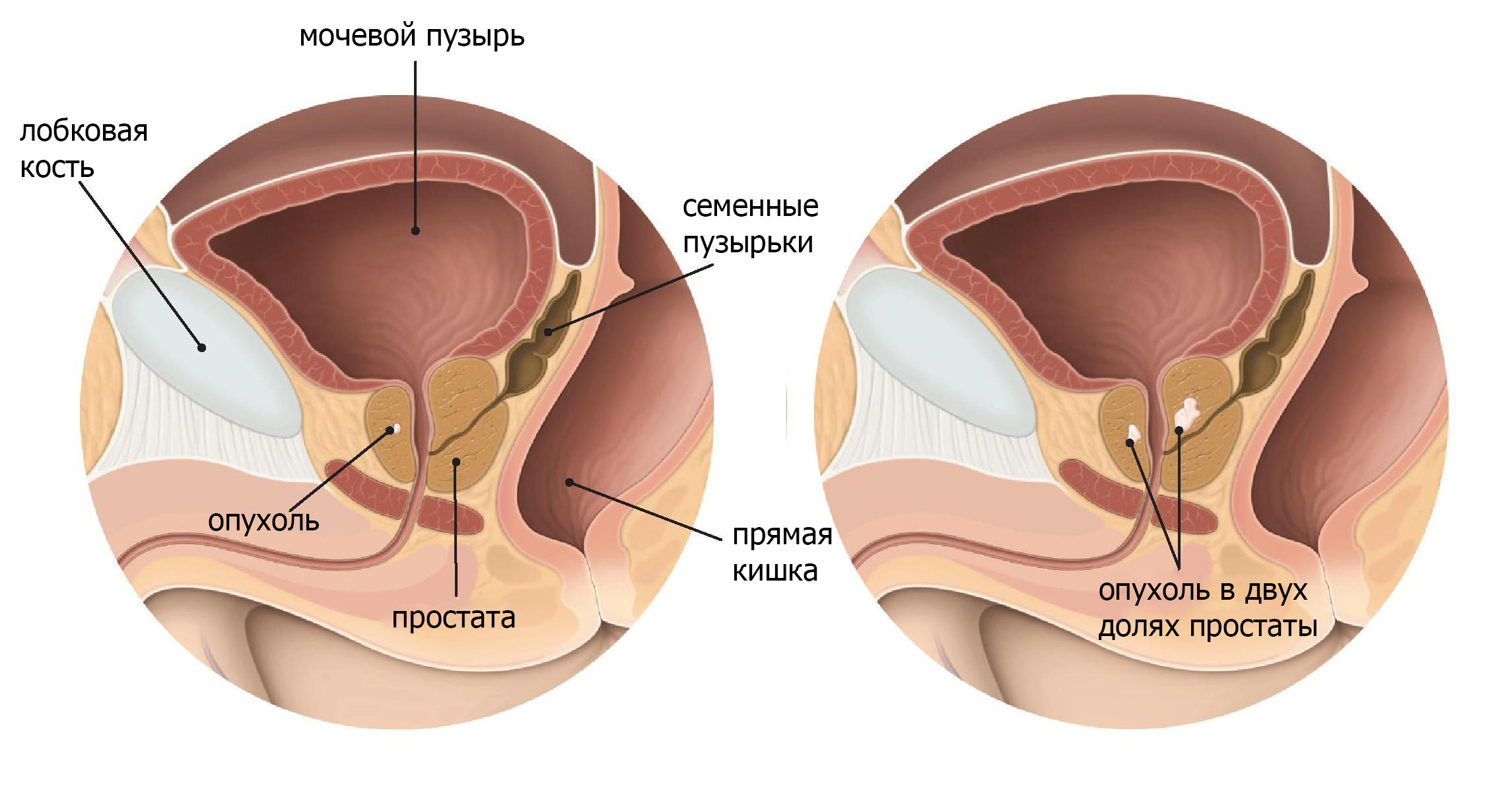
Рис. 1 T1 малая опухоль простаты которую нельзя обнаружить при ректальном исследовании Рис. 2 Т2 Опухоль простаты ограничивающаяся железой
Варианты лечения
Наиболее распространенными вариантами лечения локализованного рака предстательной железы являются: консервативное лечение, радикальная простатэктомия и лучевая терапия. Вариант лечения подходящий вам зависит от:
- характеристик опухоли;
- вашей истории болезни;
- вашего возраста;
- возможностей вашего стационара;
- ваших личных предпочтений и ценностей;
При консервативном лечении контролируется рост опухоли и рекомендуется дальнейшее лечение, при необходимо. Данное лечение обычно применяется при низкой оценке по Глисону.
Радикальная простатэктомия — это хирургическое лечение, при котором удаляется вся простата и семенные пузырьки.
Врач может также рекомендовать лучевую терапию. Эта терапия повреждает и убивает раковые клетки.
Консервативная терапия — это тип лечения, при котором ведется постоянный контроль за состоянием опухоли.
Во время активного наблюдения контролируется опухолевый рост, составляется график посещения врача. Во время каждого визита проводится несколько анализов, включая измерение уровня ПСА в крови. Цель состоит в том, чтобы перейти на другие варианты лечения, если есть признаки прогрессирования заболевания. Активное наблюдение – вариант лечения обычно применяемый при низкой оценке по Глисону. Если у вас локально распространенный рак предстательной железы, рекомендуются другие методы лечения. Цель метода состоит в том, чтобы перейти на другой варианты лечения только при появлении симптомов. Врач может рекомендовать активное наблюдение, если другие варианты лечения не подходят в вашей конкретной ситуации. Обсудите с врачом преимущества и недостатки консервативной терапии, если этот метод вам подходит.
Радикальная простатэктомия является хирургическим вариантом лечения локализованного рака предстательной железы. Цель состоит в том, чтобы удалить всю простату и семенные пузырьки. Для проведения радикальной простатэктомии используется общая анестезия. Обсудите с врачом преимущества и недостатки радикальной простатэктомии, если этот метод вам подходит.
Как проводится радикальная простатэктомия?
Радикальная простатэктомия может быть выполнена как открытым, так и лапароскопическим способом. При открытой хирургической операции доступ к предстательой железе осуществляется через брюшную стенку или промежность. Простата и семенные пузырьки удаляются, а мочевой пузырь и мочеиспускательный канал соединяются вместе (рис.3). Вводится уретральный катетер, для адекватного опорожнения мочевого пузыря и заживления места соединения уретры и мочевого пузыря. Обычно катетер удаляется через 7 дней.
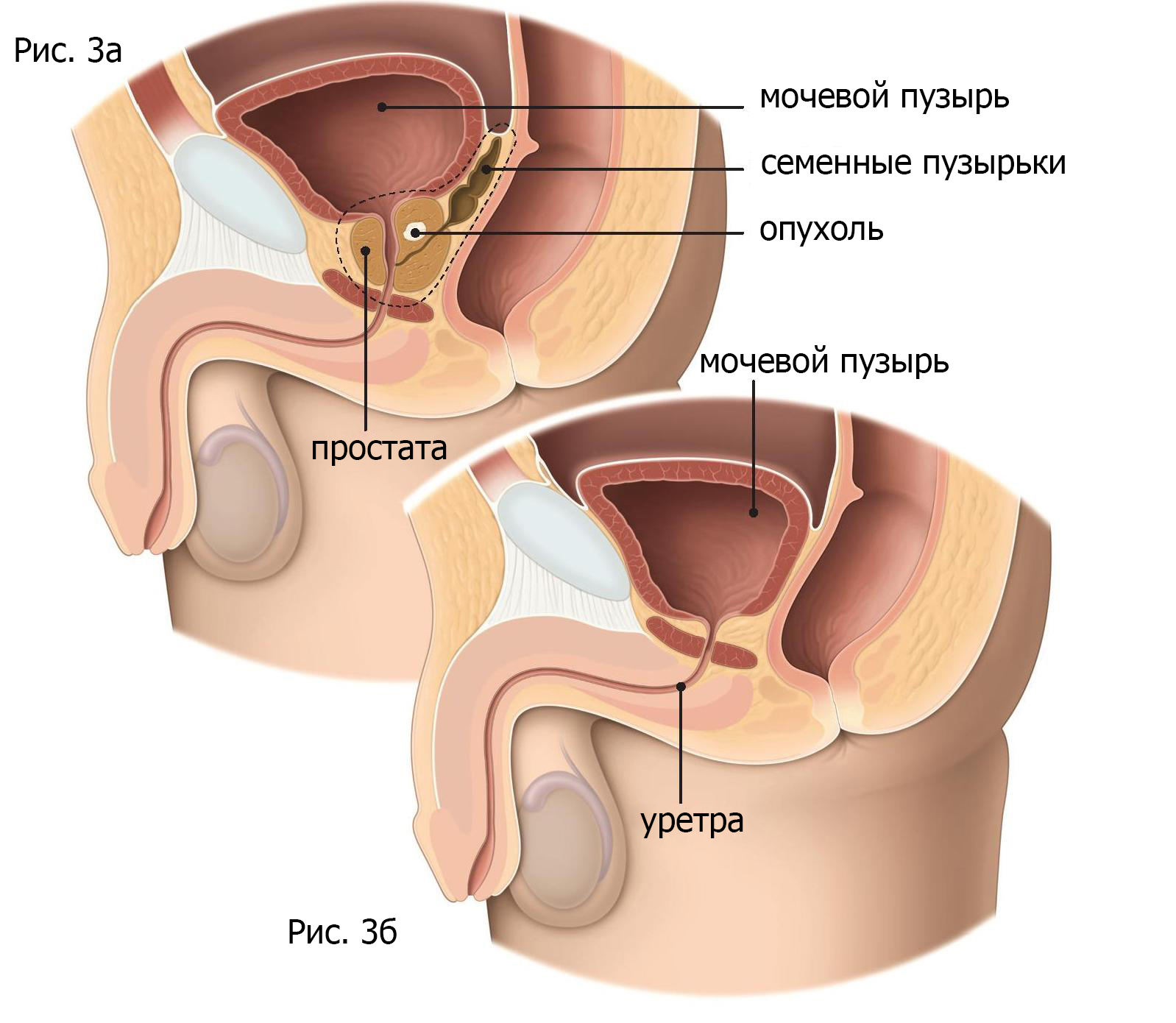
Рис. 3а – место радикальной простатэктомии с семенными пузырьками. Рис. 3б – положение мочевого пузыря после радикальной простатэктомии.
При лапароскопической операции через брюшную стенку вставляются специальный порты (трубки). Через эти порты заводятся специальные инструменты, необходимые для удаления простаты. Один порт используется для вставки камеры, которая позволяет хирургу видеть высококачественное изображение вашей простаты на мониторе. Лапароскопическая операция также может быть выполнена с помощью хирургической робототехнической системы. Для удаления локализованной опухоли предстательной железы с радикальной простатэктомией открытая и лапароскопическая операции одинаково эффективны.
Если рак распространяется на лимфатические узлы в области таза, врач может принять решение о удалении тазовых лимфатических узлов во время радикальной простатэктомии.
Как подготовиться к процедуре?
Врач объяснит, как именно в вашей ситуации необходимо готовиться к данной операции.
Нельзя кушать, пить, курить за 6-8 часов до операции. Если вы принимаете какие-либо лекарственные препараты, сообщите об этом своему врачу. Возможно, потребуется отмена некоторых препаратов за несколько дней до операции.
Обычно вы можете быть выписаны из стационара на 3 — 7 сутки после операции. Продолжительность вашего пребывания в стационаре зависит от конкретной сложившейся ситуации. Вы можете испытывать незначительные боли в нижней части живота в течение нескольких недель после открытой радикальной простатэктомии. После операции может быть недержания мочи или эректильная дисфункция. Может потребоваться лечение при таких осложнениях.
Вам необходимо вернуться в больницу, если есть:
- высокая лихорадки
- большая кровопотеря
- сильная боль
- проблемы с мочеиспусканием
Радикальная простатэктомия-стандартная операция для локализованного рака простаты. Радикальная простатэктомия может стать причиной стрессового недержания мочи (СНМ). Это происходит потому, что простата окружает мочеиспускательный канал, помогая ему противостоять давлению при полном мочевого пузыря. Если предстательная железа удалена, это может отразиться на способности уретры удерживать мочу при полном мочевом пузыре. Есть несколько вариантов лечения СНМ.
Еще один распространенный риск радикальной простатэктомии является эректильная дисфункция. Во время операции хирург должен манипулировать вблизи нервов и сосуды пениса стараясь оставить их неповрежденными. Сохранность нервов и сосудов зависит от агрессивности рака, и его распространения.
При необходимости, врач порекомендует лечение СНМ или эректильной дисфункция. Не стесняйтесь сообщать врачу о своих проблемах.
Имейте в виду, что основной целью радикальной простатэктомии является удаление опухоли
После радикальной простатэктомии при раке предстательной железы необходимо регулярное посещение лечащего врача. Регулярное наблюдение длится не менее 5 лет. Во время каждого визита проводится исследование уровня простатспецифического антигена (ПСА) в крови. В некоторых случаях может потребоваться пальцевое ректальное исследование. Последующее наблюдение важно для контроля вашего состояния после операции, чтобы обратить внимание на общее состояние здоровья и выявить возможные рецидивы рака.
Если после операции наблюдения повышение уровня ПСА, это значит, что рак предстательной железы не был полностью удален, может потребоваться дополнительное лечение для удаления всех опухолевых клеток.
Лучевая терапия повреждает и убивает раковые клетки. Раковые клетки предстательной железы обычно чувствительны к лучевой терапии. Благодаря новейшим технологиям, этот метод стал эффективным при лечения локализованного рака предстательной железы. Обсудите с вашим врачом преимущества и недостатки лучевой терапии, если этот метод вам подходит.
Цель лучевой терапии в том, чтобы убить раковые клетки в простате. Поскольку излучение может затронуть клетки других органы, такиех как мочевой пузырь, важно, чтобы пучок излучения был нацелен на раковые клетки. В настоящее время лучевая терапия имеют повышенную точность луча, и позволяет использовать более высокие дозы радиации с меньшим количеством побочных эффектов. Стандартный курс лучевой терапии (Рис. 4) длится около 8 недель, 5 дней в неделю. Вы получаете одну дозу радиации в день. Процедура занимает около 20 минут каждый день.
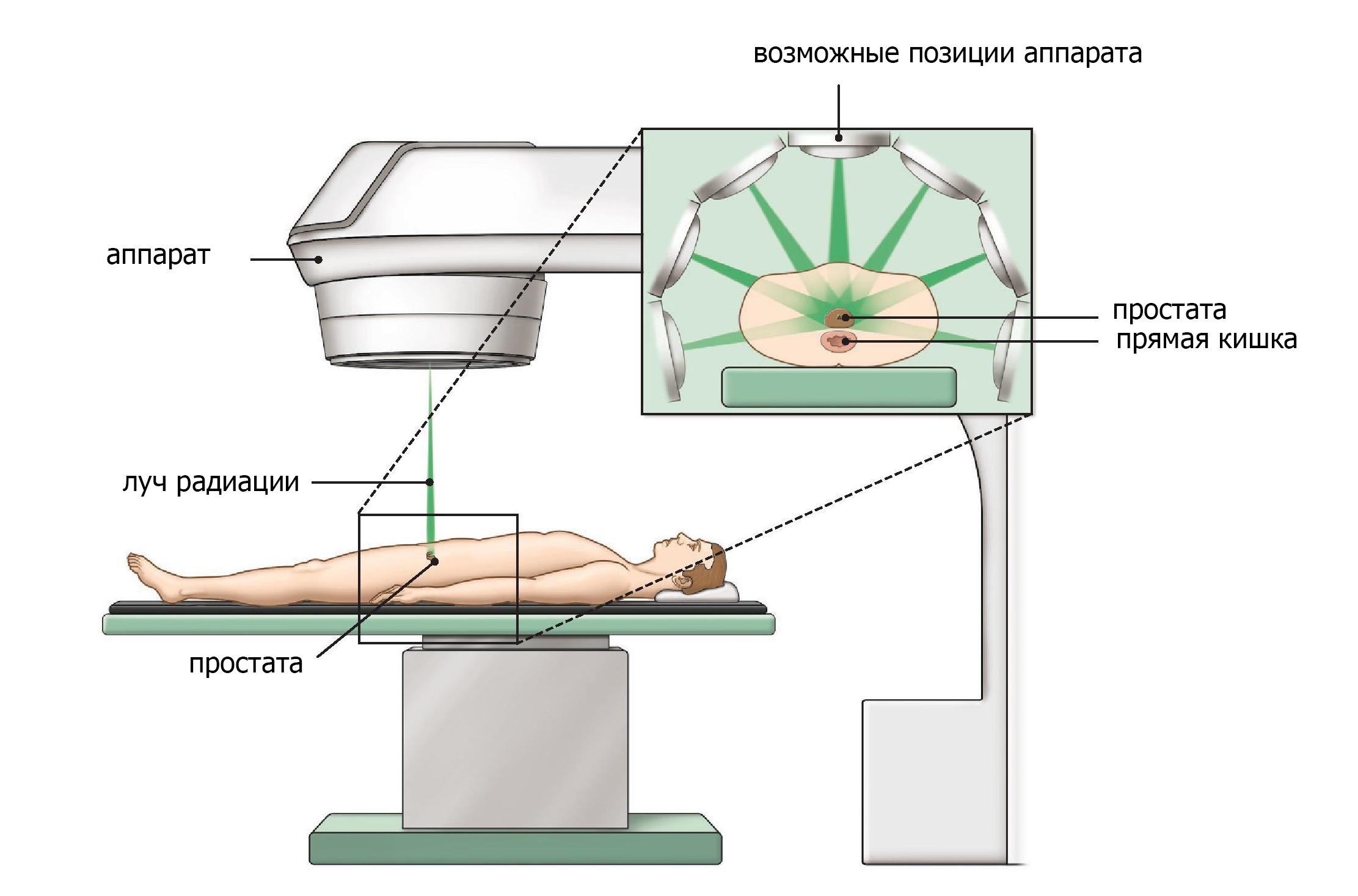
Рис. 4 Внешняя лучевая терапия
Перед началом курса лучевой терапии необходимо выполнение КТ. Это делается для более точного определения области, которая будет подвергаться излучению, а также окружающей ткани, которую не следует затрагивать. В последние годы лучевая терапия с использованием визуализации стала более доступной. Для данной терапии онколог очень точно определяет место опухоли с помощью рентгеновского или компьютерного исследования, чтобы убедиться, что доза облучения доставляется точно. Другой формой лучевой терапии является внутренняя лучевая терапия (брахитерапия). Для этого типа лечения источник излучения подводится непосредственно к простате (рис.5). Ваш врач может предложить такой вариант лечения, если у вас низкий балл по Глисону и нет никакой симптоматики.
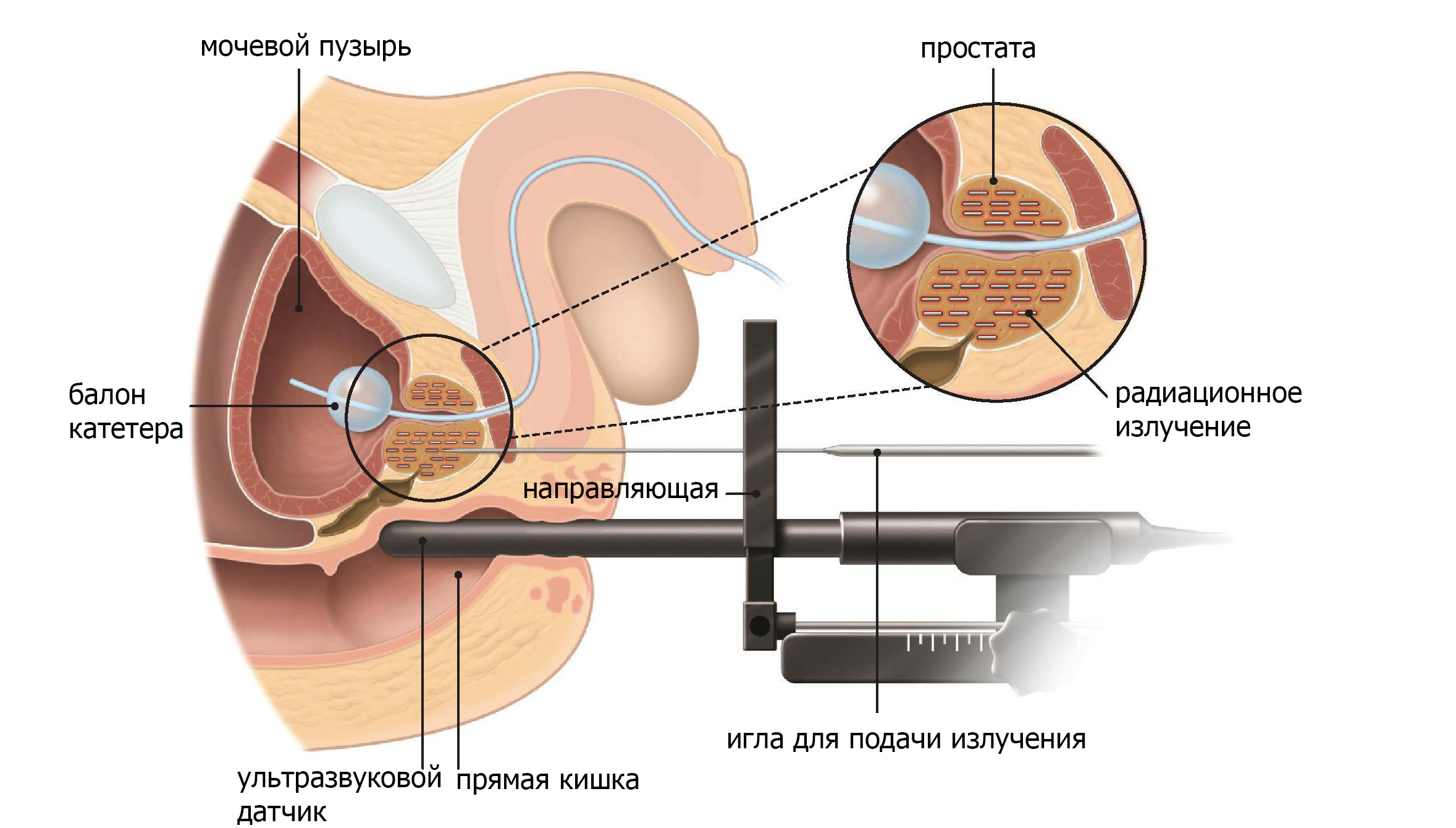
Рис. 5 Брахитерапия.
Врач объяснит, как именно в вашей ситуации необходимо готовиться к данной процедуре.
Будет составлено расписание приемов пищи и жидкости перед каждой процедурой, чтобы убедиться, что ваш мочевой пузырь адекватно наполнен, а прямая кишка пуста. Если вы принимаете какие-либо лекарственные препараты, сообщите об этом своему врачу.
Как правило, вам не нужно прекращать прием препарата во время лучевой терапии.
Общие побочные эффекты — жжение при мочеиспускании, учащенное мочеиспускание и раздражение анального отверстия. Это связано с тем, что окружающие органы, особенно мочевой пузырь и прямая кишка, также получают небольшую дозу облучения. Обычно эти симптомы появляются на середине курса лечения и исчезают через несколько месяцев после его окончания.
Общим побочным эффектом лучевой терапии является кровотечение в мочевом пузыре и прямой кишке, даже через несколько лет после лечения. Вы также можете испытать симптомы нижних мочевых путей (СНМП) или эректильную дисфункцию. Побочные эффекты лучевой терапии варьируются связаны с состоянием вашего здоровья и типом лучевой терапии, которую вы получаете.
После радикальной простатэктомии при раке предстательной железы необходимо регулярное посещение лечащего врача. Регулярное наблюдение длится не менее 5 лет. Во время каждого визита проводится исследование уровня простатспецифического антигена (ПСА) в крови. В некоторых случаях может потребоваться пальцевое ректальное исследование. Последующее наблюдение важно для контроля вашего состояния после операции, чтобы обратить внимание на общее состояние здоровья и выявить возможные рецидивы рака.
Если у вас локализованный рак предстательной железы с высоким показателем Глисона, врач может рекомендовать лучевую терапию в сочетании с гормональной терапией. Ваш врач подробно объяснит, как нужно должны подготовиться к такому лечению.
Если после операции наблюдения повышение уровня ПСА, это значит, что рак предстательной железы не был полностью удален, может потребоваться дополнительное лечение для удаления всех опухолевых клеток. Обсудите с вашим врачом, какой вариант лечения для вас наиболее подходит.
Помимо хирургии, лучевой терапии и консервативного лечения существуют и другие варианты лечения локализованного рака предстательной железы, такие как:
- Криохирургическая аблация предстательной железы (CSAP)
- Ультразвуковое исследование с высокой интенсивностью фокусировки (HIFU)
- Фокальная терапия
Криохирургическая аблация предстательной железы (CSAP) является экспериментальной методикой лечения рака предстательной железы. Это минимально инвазивная операция, при которой воздействует низкой температцрой на опухолевые клетки, чтобы убить их (рис. 6).
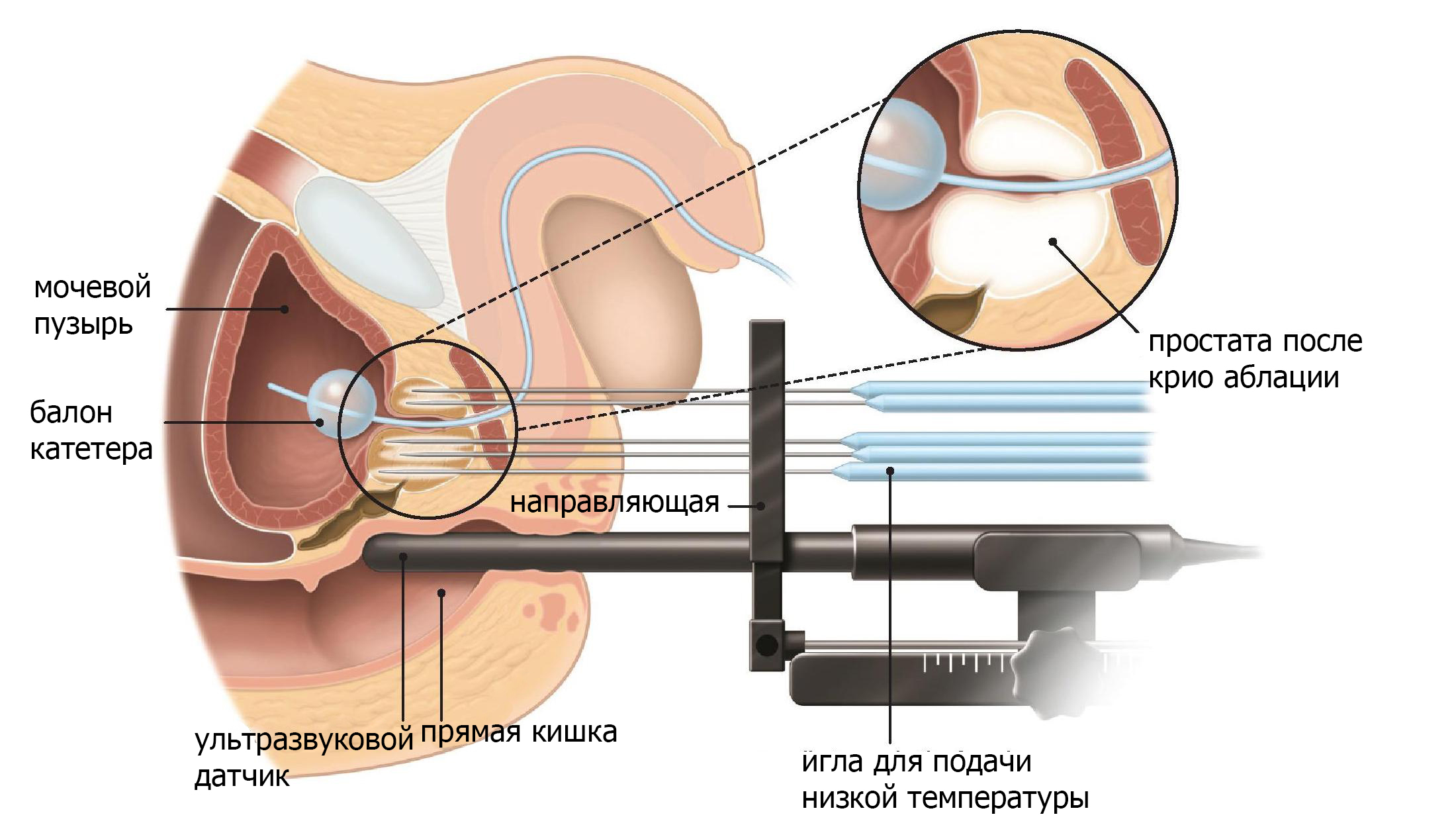
Рис.6 Криохирургическая аблация предстательной железы (CSAP)
Высокоинтенсивный фокусированный ультразвук (HIFU) — экспериментальная методика лечения рака предстательной железы. Он использует энергию высокочастотных звуковых волн для нагрева раковых клеток и их уничтожения (рис.7)
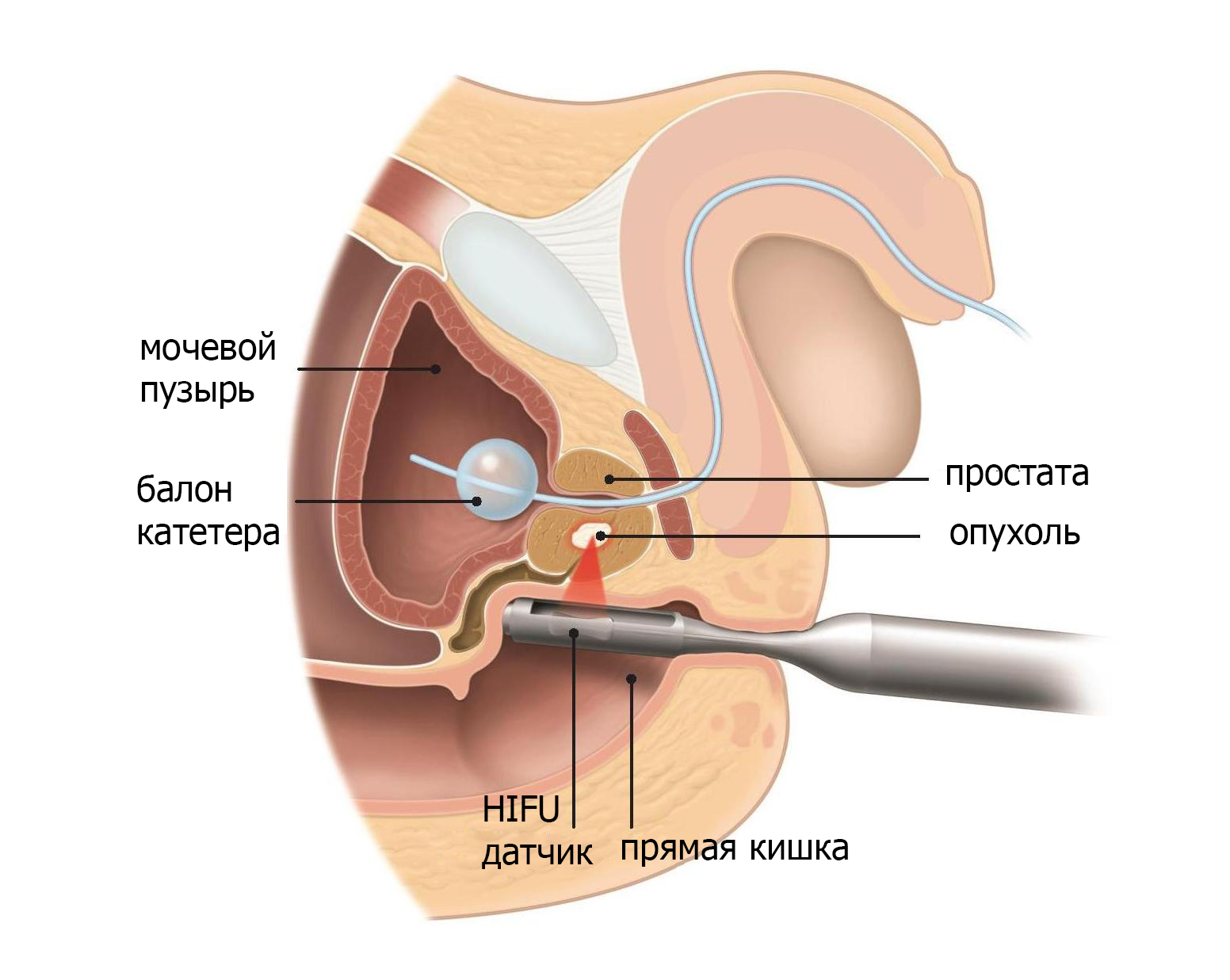
Рис. 7 Высокоинтенсивный фокусированный ультразвук (HIFU) для лечения рака простаты.
Фокальная терапия — термин для нескольких экспериментальных методов, чтобы разрушить маленькие опухоли в предстательной железе. Поскольку метод нацелен непосредственно на раковые клетки, нет никаких повреждений других тканей простаты или нижних мочевых путей (рис.8)
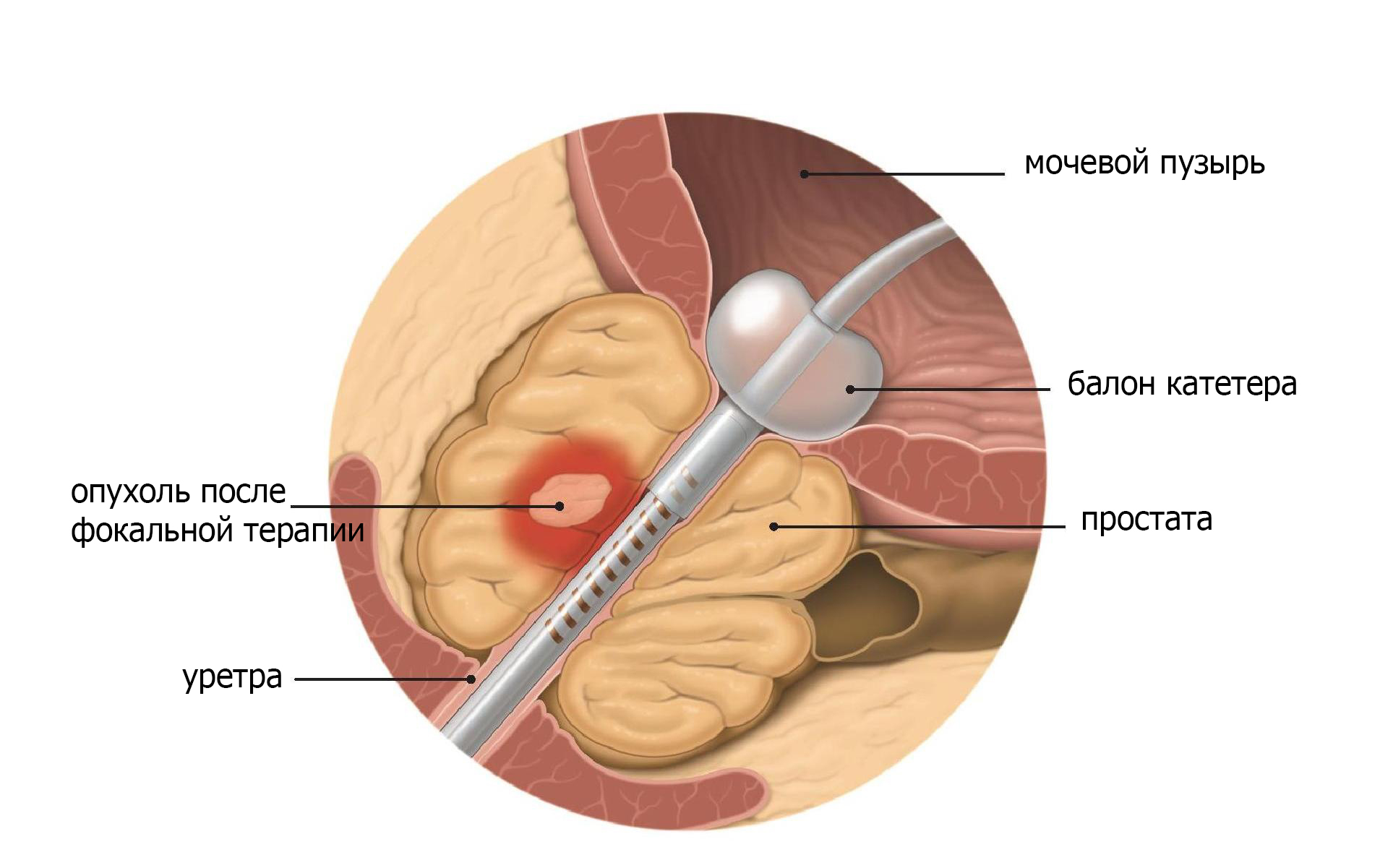
Рис. 8 Фокальная терапия
Врач обсудит эти варианты лечения, если другие методы вам не подходят. Это также зависит от ваших личных предпочтений и ценностей, а также оснащения отделения. Вам может быть предложено такое лечение как часть клинического испытания.
Возможно, что рак предстательной железы возникает после лечения. Это называется рецидивом. Рак может возникнуть в простате, в ткани вокруг простаты или тазовых лимфатических узлах или в других органах. Дальнейший путь лечения зависит от месторасположения опухоли. Врач будет порекомендовать проведение дополнительных методов исследования, таких как компьютерная томография, МРТ, или остеосцинтиграфия, чтобы определить местонахождение опухоли, определить ее характеристики и решить тактику лечения. Если у вас была радикальная простатэктомия и уровень ПСА в крови повысился, это может быть признаком рецидива. Врач может порекомендовать лучевую терапию. Данная процедура будет направлена на область, где была расположена простата, чтобы убить раковые клетки. Если у вас была лучевая терапия, то может быть рекомендована радикальная простатэктомией. Если вы лечились экспериментальными методами, посоветуйтесь со своим врачом, какой вариант лечения вам подойдет лучше всего.
Подготовка к консультации может быть очень полезной. Это поможет вам и вашему врачу лучше понять проблему и подобрать правильный вариант лечения. Это также поможет вам подготовиться к лечению и возможным побочным эффектам.
Вот несколько вещей, которые вы можете сделать:
- Запишите вопросы, которые вы хотели бы задать врачу. Это поможет вам вспомнить то, что вы хотите спросить.
- Узнайте информацию о вашем конкретном типе рака простаты.
- Если доктор использует термины, которые вы не понимаете, попросите объяснить их.
- Если вы принимаете какие-либо лекарственные препараты, сообщите об этом своему врачу. Некоторые из этих лекарств могут влиять на лечение
Радикальная простатэктомия может вызывать стрессовое недержание мочи (СНМ). Это означает, что моча может произвольно подтекать во время кашляя, смеха, бега, подъема по лестнице и т.д. Вот несколько советов, которые помогут вам справиться с этими симптомами:
- Старайтесь всегда знать, где находится ближайший туалет. Никогда не бойтесь и не стесняйтесь спрашивать, где туалет, когда вы находитесь вдали от дома
- Если у вас есть проблемы с подтеканием мочи, вы можете использовать пенильные зажимы или прокладку. Пенильные зажимы надеваются поверх пениса и удерживают мочу.
- Используйте средства борьбы с неприятным запахом. Спросите о таких в аптеке.
- Носите одежду темного цвета. На светлой одежда могут появляться пятна.
- Носите свободную и комфортную одежду
- Имейте дополнительный комплект одежды под рукой
Другой распространенный риск операции — эректильная дисфункция. Существуют различные варианты лечения этого состояния. Наиболее распространенными из них являются: таблетки, инъекции или протезирование. Обсудите с врачом какой вариант больше вам подходит.
СНМ или эректильная дисфункцией после радикальной простатэктомии могут трудно поддаваться лечению. Что оказывает пагубное психологическое воздействие.
Поддержка во время лучевой терапии.
Во время лучевой терапии вы можете заниматься своей повседневной деятельностью. Лечение может повлиять на нижние мочевые пути, кишечник, и может вызывать усталость. Усталость может быть результатом ежедневных поездок в больницу. Обычно эти симптомы исчезают через несколько месяцев после лечения.
Из-за излучения может быть повреждена кожа. Чтобы ухаживать за кожей, вы можете:
- Избегать повреждения облучаемой области.
- Используйте лосьон для кожи для борьбы с раздражением.
- Избегайте воздействия прямых солнечных лучей.
- Используйте солнцезащитный крем с высоким фактором. Носите одежду из хлопчатобумажной или льняной ткани;
- Ежедневно соблюдайте правила личной гигиены;
- Осторожно вытерайте кожу после мытья;
- Не посещайте баню, сауну
После операции или лучевой терапии будет составлен график посещений для наблюдения за вашим состоянием. Частота посещений и дополнительные исследования зависят от вашего заболевания.
Важно придерживаться графика. Во время этих наблюдений врач следит за вашим состоянием и может своевременно обнаружить рецидив опухоли. Необходимо сообщить врачу, если у вас появились новые симптомы, которые могут быть связаны с раком предстательной железы.
Важно поддерживать здорового образа жизни во время и после лечения. Старайтесь регулярно выполнять физические упражнения. Либо обратитесь к физиотерапевту. Попытайтесь сбалансировать диету с содержанием овощей, фруктов и молочных продуктов. Также включите продукты содержащие крахмал, такие как хлеб, картофель, рис, макароны, а также богатые белками продукты, такие как мясо, рыба,яйца или бобовые. Попытайтесь меньше есть сахара, соли и жирной пищи. Можете обратиться к диетологу. Попробуйте бросить курить. Это может помочь вам быстрее восстановиться после лечения.
После лечения вас может беспокоить дальнейший прогноз, влияние рака на вашу социальную, бытовую, финансовую ситуацию. Обычно беспокоит мысль о рецидиве рака. Если вас это беспокоит, обратитесь к своему врачу и узнайте о риске рецидива. Во время лечения вы будете не работоспособны, поэтому обсудите со своим начальствам все аспекты и время возвращения к рабочей деятельности. Обсудите со своей страховой компанией финансовую поддержку вашего лечения
Источник
Комментарии
| »» Содержание | Б.П. Матвеев, Б.В. Бухаркин, В.Б. Матвеев |
Глава 6. Лечение рака предстательной железы
Лечение рака предстательной железы, так же, как и всех онкологических заболеваний, определяется стадией болезни. Однако если в отношении больных с местнораспространенной опухолью или с уже имеющимися метастазами существует более или менее единый подход, то в лечении начальных стадий (Т1-Т2) рака предстательной железы единой точки зрения нет. В настоящее время больному может быть предложено три варианта лечения:
1) радикальная простатэктомия;
2) радикальная лучевая терапия;
3) выжидательная тактика (табл. 22).
Таблица 22. Методы лечения локализованного рака предстательной железы.
1. Радикальная простатэктомия
2. Лучевая терапия
а) наружная
б) внутритканевая
3. Отсроченное лечение
4. Методы в стадии разработки
а) криотерапия
б) лазеротерапия
с) сфокусированный ультразвук высокой интенсивности
Больных раком предстательной железы невозможно подвести под одну схему лечения (табл. 23). Подход во многом должен быть индивидуальным. Остановимся подробно на всех применяемых методах лечения.
Таблица 23. Алгоритм диагностики, определения стадии и лечения рака предстательной железы.
Лечение локализованного рака предстательной железы (Т1-2).
С усилением скринингового контроля населения и внедрением современных методов диагностики (определение простатоспецифического антигена, трансректального УЗИ, магнитного резонанса с использованием ректальных датчиков и т.д.) число впервые диагностированных случаев заболевания раком предстательной железы быстро увеличивается. Естественно, что при этом значительно возросло количество больных с локализованным раком предстательной железы, причем задолго до того, как у них появятся клинические проявления болезни. Увеличение количества вновь выявленных больных, однако не привело к увеличению смертности. Это наглядно отражено в табл. 24 с приведенными данными США.
Таблица 24. Случаи заболевания, смертности и летальности раком предстательной железы в США.
| 1985 | 1991 | 1993 | |
| Заболеваемость (кол-во) | 76.000 | 122.000 | 169.000 |
| Смертность (кол-во) | 27.000 | 32.000 | 34.000 |
| Летальность (%) | 35 | 26 | 20 |
Приводимая статистика вызвала много вопросов, но основной из них: не породила ли ранняя диагностика риск «сверх лечения», так как многие из вновь выявленных случаев рака предстательной железы, даже не леченные, не вызовут смерти больного. Этот же вопрос возникает при сравнении выживаемости у леченных и нелеченных больных начальными стадиями заболевания. Остановимся подробнее на применяемых методах лечения локализованного РПЖ.
Отсроченное лечение. Выжидательная тактика при раке предстательной железы, которая заключается в том, что лечение начинается с появлением клинических симптомов заболевания, до сих пор остается спорной. Если в США стандартным лечением для локализованного рака простаты является простатэктомия или лучевая терапия, отсроченное лечение без первичной терапии практиковалось в Европе, большей частью в Скандинавских странах, где самый высокий уровень заболевания РПЖ.
Наиболее достоверное и хорошо документированное исследование по отсроченному лечению представляет сообщение из Швеции Johansson J. (1994). С марта 1977 по февраль 1994 г. было выявлено 654 больных, но в исследование было взято 223. Первоначально брали больных, у которых опухоль локализовалась лишь в железе и не прорастала капсулу (Т0-Т2) и не выявлялись отдаленные метастазы. Решено было брать только больных с высокодифференцированным раком и моложе 75 лет. В среднем больные наблюдались 12.5 лет. За время наблюдения прогрессирование заболевания отмечено всего лишь у 77 (35%) больных, а умерло 148 (66%), но из них только 23(10%) умерли от рака предстательной железы. Риск прогрессирования и смерти от рака предстательной железы был значительно выше при малодифференцированном раке (3-я гистологическая стадия), нежели при высокодифференцированном. Уровень прогрессирования рака был наибольшим в первые 5 лет (68%) а к 10 годам снизился до 55%. И самое интересное в том, что уровень безметастатической выживаемости был 90% через 5 лет и 83% через 10 лет. Сравнивая полученные данные с литературными, автор отмечает, что 10-летняя выживаемость при простатэктомии равна 93%, при отстроченном лечении — 84% и при лучевой терапии — 74%. Однако подчеркивается, что не существует значительных критериев в пользу того или иного метода лечения, а руководствоваться надо прежде всего качеством жизни. Приведенное исследование Johansson J., хотя и дает очень интересные результаты, но далеко не бесспорно, так как у большей части больных (146 из 223) была высокодифференцированная форма рака предстательной железы, а средней возраст пациентов был 72 года (на этом мы остановимся далее более подробно). Для более четкого представления об отсроченном лечении приводим сводные данные различных авторов, собранные Adolfson J. (1995) (табл. 25).
Таблица 25. Выживаемость больных раком предстательной железы начальных стадий после отсроченного лечения.
| Автор | n | Стадия | Выживаемость в % | ||
| 5 лет | 10 лет | 15 лет | |||
| Moskovitz et al., 1987 | 44 | T1-2 | 61% | 34% | — |
| Graverson et al., 1990 | 50 | T1-2 | 70% | 55% | 32% |
| Johansson et al., 1992 | 117 | T1-2 | 63% | 40% | — |
| Johansson et al., 1992 | 58 | T0-2 | 78% | 58% | — |
| Adolfsson et al., 1991 | 61 | T1-2 | — | 85% | — |
| Adolfsson et al., 1992 | 122 | T1-2 | — | 51% | — |
| Chisholm et al., 1992 | 107 | T0-1 | 65% | 48% | — |
| Stenziet al., 1993 | 34 | T0-2 | 67% | 34% | — |
| Warner & Whilmore | 68 | Тв | — | 72% | 46% |
Как видно из представленной таблицы, десятилетняя выживаемость при отсроченном лечении у различных авторов колеблется от 85% до 34% .
Суммируя все последние публикации, следует сказать, что выжидательная тактика целесообразна у больных пожилого возраста при высокодифференцированных опухолях небольшой величины (Т0-Т2). Особенно это касается больных, имеющих тяжелые сопутствующие заболевания. Такие больные нуждаются в постоянном наблюдении с контролем за уровнем ПСА. Такой же подход возможен у пожилых людей с более крупными опухолями (Т3), так как результаты долгосрочных исследований свидетельствуют о низкой частоте метастазирования у таких больных.
Выжидательная тактика особенно касается людей пожилого и старческого возраста, у которых по прогнозам не ожидается долгой продолжительности жизни с момента выявления заболевания, поскольку у них часто имеются тяжелые сопутствующие заболевания. Однако больным и членам их семей необходимо разъяснять, какие соображения заставляют откладывать активное лечение.
По результатам последних исследований при выжидательной тактике высокодифференцированные опухоли (число баллов Глисона 2-4) метастазируют в 2.1% случаев в год, агрессивные опухоли (число баллов Глисона 7-10) — в 13.5% случаев в год. Больные с опухолями низкой градации живут более 10 лет в 87% случаев; больные с низкодифференцированными опухолями — в 26% случаев.
Лучевая терапия при локализированном раке предстательной железы.
Лучевая терапия при локализованных формах рака предстательной железы применяется уже много лет как метод радикального лечения и в определенной степени является конкурирующим с простатэктомией. Особенно лучевая терапия имеет преимущество у больных с тяжелыми сопутствующими заболеваниями, которые являются противопоказаниями к хирургическому лечению. Важно подчеркнуть, что выживаемость после лучевой терапии близка к таковой после радикальной простатэктомии.
Таблица 26. Критерии отбора больных раком предстательной железы для лучевой терапии.
- Гистологическая верификация рака предстательной железы
- Ограниченный местный рост опухоли
- Достаточная ожидаемая продолжительность жизни, при которой целесообразны попытки полного излечения
- Отсутствие патологии нижнего отдела мочевых путей (особенно обструкции мочевых путей)
- Отсутствие вовлечения в опухолевый процесс ободочной и прямой кишки
Однако следует отметить, что оба метода радикального лечения рака предстательной железы имеют свои преимущества и недостатки (табл. 27, Kirbi, 1997).
Выживаемость после лучевой терапии по литературным данным достигает 15 лет в 40-60% случаев. Это вполне хорошие результаты, и мы еще вернемся к этому вопросу, особенно если учесть, что лечению подвергаются в основном больные старше 60 лет. Получаемые после лечения осложнения чаще всего связаны с дизурией, вплоть до недержания мочи. Очень редко возможно сморщивание мочевого пузыря, гематурия и поражение прямой кишки.
Таблица 27. Преимущества и недостатки лучевой терапии и радикальной простатэктомии в лечении ограниченного рака предстательной железы.
Лучевая терапия
Преимущества:
Недостатки:
— поражение прямой кишки (5-10%)
— недержание мочи (- импотенция (20-30%)
— поражение мочевого пузыря (10-20%)
— гематурия (5-10%)
Радикальная простатэктомия
Преимущества:
Недостатки:
— импотенция (> 50%)
— тяжелое недержание мочи (- тромбоэмболия легочной артерии (- повреждение прямой кишки (- стриктура мочеиспускательного канала (- кровотечение ( Литература
Заридзе Д.Г. Эпидемиология рака простаты. В материалах Европейской гистомы онкологов. Рак простаты. Москва. 1997.
Шолохов В.Н. Роль и место ультразвуковой томографии в диагностике рака предстательной железы. Материалы Европейской школы онкологов «Рак простаты» Москва, 1997.
Armstrong В. and Doll R. Environmental factors and cancer incidence and mortality in different countries,with special reference to dietary practices. Int. J. Cancer, 15, 617-631, (1975).
Armitage T.Y., Cooper E.H., Hewling D.W. et al. The value of the measurement of serum prostate specific antigen in patients with benign prostatic hiperplasia and untreated prostate cancer. Br. Y. Urology, 1998, 62, N6, 584-589
Benson N.C., Wang I.S., Pontuck K.A. et al. Prostate specific antigen density: a means of distinguishing benign prostatic hypertrophy and prostate cancer. J Urol. 1992, 147:815.
Boyle P., Zaridze D.G. Risk factors for prostate and testicular cancer. Eur. J. Cancer, 29A, 7, 1048-1055 (1993).
Blhtestein D.L, Bostwick D.C., Bergstralh E.J. et al. Eliminating the need for bilateral pelvic lymphadenectomy in select patients with prostate cancer. J. Urol. 1994: 151: 13;15.
Brawer M.K., Chetner M.P., Beatie J. et al. Screening for prostate carcinoma i: with prostate-specific antigen. J. Urol. 1992; 147:841
Catalona W.J., Smith D.S., Ratliff T.L. et at. Measurement of prostate- specific antigen in serum as a screening test for prostate cancer. N Engi J Med 1991; 324:1156
Catalona W.J., Smith D.S., Ratiiff T.L. et al. Detection of organ-confined prostate cancer is increased through prostate specific antigen-based screening. JAMA 1993; 27:948
Epstein. Y. Critical issues in grading of adenocarcinomas of the prostate. The Canadian journal of urology June 1997, Supplement 2, 28-33
Ghadirian P., Cadotte M., Lacroix A., Perret Ch. Family gregation of cancer of the prostate in Quebec: The tip of the iceberg. The Prostate, 19,43-52 (1991).
Hill P., Wynder L, Garnes H. and Walker A.R.p. Environmental factors, hormones status and prostatic cancer. Prev. Med., 9, 657-666, 1980.
Hudson M.A., Bohnson R.R., Catolona W.Y. Clinical use of prostate specific antigen in patientswith prostaticcancerY, Urd., 1989, 142, 1011-1017.
Jong F.H., Oishi К., Hayes R.B., Bogdanovicz J., Raatgever J., Maas P.J. van der Yoahima O., Schroder F.H. Peripheral hormone levels in controls and patientswith prostatic cancer or benign prostatic hyperplasia: results from the Dutch-Japanese case-control study. Submitted (1990).
Kabalin J.N., McNeal J.E. et al. Unsuspected adenocarcinoma of the prostatients Undergoing cystoprostatectomyfor other causes: incidence, histology and morphometric observations. J. Urol. 1989; 141:1091
Kapish J., Flooner W.J. et al. Serum PSA adjusted for volume oftrabsition zone /PSAT/ is I ore accurable then PSA adjusted for total gland volune /PSAD/ in detecting adenocarcinoma of the prostate. Urology 1994; 43:601.
Kirby R.S. Pro-treatment staging of prostate cancer: recent advances and future prospects. Prostate cancer, 1997, September, 2-10. Mettlin C., Lilya H. A. Akallikrein — like serine proteas in prostate fluid cleaves the predominant seminal vesicle protein. Y. Clin. Invest., 1985, 76, 1899-1903
Kleer E., Larsen-Keller J.J., Zincke Hatal. Ability of preoperative serum serum prostate specific antigen value to predict pathologic stage and DNA ploidy: influence of clinical stage and tumor grade. Urology 1993; 40:207.
Klein H., Bressel M., Kastendieck H., Voigt K.D. Androgens, adrenal androgen precursors, and their metabolism in untreated primary tumors and lymph node metastases of human prostatic cancer. Am. J. Clin. Oncol. (CCt), II (Suppl.2), 30-36 (1988).
Mandelson M., Wagner E.H., Thompson R.S. PSA screening: a public health dilemma. Annual Review of Public Health. 16. 283- 306, 1995.
Mettlin С., Lee F. et al. The American Cancer Society. National Prostate Cancer Detection Project: findings on the detection of early prostate cancer in 2.425SL, men. Cancer 1991:67:2949-58.
Jimerican Cancer Society. National Prostate Cancer Detection Project. Cancer Suppi. 1995, Vol:75, N 7,1790:94.
Myrtle Y.F., Kimley P.Y., Yvor L.P. et al. Clinical utility of prostate specific antigen (ПСА) in the management for prostate cancer. In advances in cancer diagnosis. San Diego Hybritech Inc., 1986, 1, 1-6.
Osterling J.E., Chute C.C., et al. Longitudinal changes in serum PSA /PSAvelosity/ in a community-based cohort of men. J Urol. 1993; 193:412A.
Osterling Y.E., Yacobsen S.I., Chutte Y. et al. Serum prostate specific antigen in a community based population of healthy men: establishment of age-specific reference ranges Yama 1993, 270:860.
Oesterimg J.E., Suman V.J. et al. PSA-detected /clinical stage T1c or BO/ prostate cancer: pathologically significant tumors. Urol. Clin. North Am. 1993:20:687.
Osterling J.E. Prostate specific antigen: Its role in the diagnostic and staging of cancer: Nat. Conf. Prostate Cancer. Philadelphia, Sep. 29 — Oct. 1, 1994 Cancer. -1996. -75N7, Suppl-C1795-1804.
Fieissig IA., Klocker H. et al. Improvement of prostate cancer (PSA) screening by determination of the ratio free/total PSA in addition to PSA levels — a prospective stady. European Urology Abstracts XI 1 Congress of the European Association of Urology, 1996, Paris.
Parkin, D.M., Muir, C.S., Whelan, S.L, Gao Y.T., Ferlay J., (eds), Powel J. Cancer Incidence in Five Continents, vol. VI, IARC Scientific Publication, N20, Lyon (1992).
Partin A.W., Carter H.B., Chan D.W., et al. Prostate specific antigen in the staging of localized prostate cancer influence of tumor volume and benign hyperplasia. J Urol: 1990; 143:747
Partin A.W, Yoo J., Carter H.B. et al. The use of prostate specific antigen clinical stage Gleason and reason score to predict pathological stage in men with localized te cancer. J. Urol. 1993:150:110.
Pohan Т.Е., Howe G.R., Burch J.D., Jain M. Dietary factors and risk of prostate cancer: a case-control study in Ontario, Canada. Cancer /Causes/ Control, 6, 145-154(1995).
Scaletsky R., Koch M.O., Eckstein C.W. et al., Pathologic findings in prostatecancer detected because of PSA elevation. J. Urol. 1993; 149:303A.
Stamey T.A., Yong N., Hay A.R. et al. Prostate — specific antigen as a serum marker for adenocarcinomaofthe prostate. New Engl., Y. Med. 1987, 317, 909-916/. Carter H.B., Pearson J.D., Wacliwew X. et al. PSA variabilityin menwith BPH. Jtirol. 14;151:312A.
Stenman X.J.H., Leinonen J. et al. A complex between prostate-specific antigen and alphi-I-antidiomotrypsin is the major form prostate-specific antigen in serum of patients with prostatic cancerassay of the complex improves clinical sensitivityfor cancer. Cancer Res. 1991; 51:222.
Talaminii R., La Vecchia C., Decarli A., Negri E., Francheschi S. Nutrition, social factors and prostatic cancer in a Northern Italian population. Br. J. Cancer, 53,817-82
Watt K.W., Lee P.Y., M. Tirnkulu. Human prostate specific antigenistructural and functional similarity with serine proteases Proc. Natl. Acad. Sci USA, 1986, 83, 3166-3170
West D.W., Sslattery M.L., Robinson L.M., French Т.К., Manoney A.W. Adult dietary intake and prostate cancer risk in Utah: a case-control study with spacial emphasis on aggressive tumors. Cancer Causes Control, 2, 85-94(1991).
Zaridse D.G., Boyle P. Cancer of the prostate: epidemiology daetiology. Brit. J. Urol., 59, 493-502(1987).
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)
Источник