Антагонист эстрогенов для лечения рака молочной железы
Описание
В качестве противоопухолевых средств в клинической практике применяют ряд гормональных препаратов — агонистов и антагонистов андрогенов, эстрогенов, гестагенов и других гормонов. Эти средства показаны преимущественно при гормональнозависимых опухолях. Гормональная противоопухолевая терапия имеет важное значение при лечении рака молочной железы, эндометрия, предстательной железы. Применяют гормональные средства также для лечения рака почки, карциноида, некоторых опухолей поджелудочной железы, меланомы и др.
Взаимодействие между гормонами и гормональнозависимыми опухолями было выявлено впервые в 1896 г., когда хирург из Глазго J. Beatson опубликовал данные успешного лечения трех женщин с прогрессирующим раком молочной железы, которым была произведена двусторонняя овариэктомия.
По механизму действия гормональные препараты отличаются от цитотоксических противоопухолевых средств. Основная их роль — восстановление нарушенной гуморальной регуляции функции клеток. Вместе с тем не исключается и специфическое влияние на опухолевые клетки: они в определенной степени тормозят деление клеток и способствуют их дифференцировке.
Эстрогены назначают для подавления действия в организме андрогенов (например, при раке предстательной железы), андрогены, напротив, — для уменьшения активности эстрогенов (при раке молочной железы и др.). При раке молочной железы и матки используют также прогестины (медроксипрогестерон).
К противоопухолевым гормональным средствам и антагонистам гормонов относят:
1. Андрогенные средства — тестостерон, метилтестостерон, дростанолон (медротестрона пропионат), пролотестон.
2. Эстрогенные средства — фосфэстрол, диэтилстильбэстрол, полиэстрадиола фосфат, эстрамустин, этинилэстрадиол, хлоротрианизен, полиэстрадиола фосфат, гексэстрол.
3. Гестагенные средства (прогестины) — гестонорона капроат, медроксипрогестерон, мегестрол и др.
4. Антагонисты эстрогенов (антиэстрогены) — тамоксифен, торемифен.
5. Антагонисты андрогенов (антиандрогены): бикалутамид, флутамид, ципротерон и др.
6. Гипоталамические факторы («рилизинг-факторы»), высвобождающие гормоны гипофиза: бусерелин, гозерелин, лейпрорелин, трипторелин и др.
7. Ингибиторы ароматазы (аминоглутетимид, анастрозол, эксеместан, летрозол).
8. Ингибиторы биосинтеза гормонов надпочечников (аминоглутетимид, митотан).
9. Глюкокортикоиды (преднизолон, дексаметазон и др.).
10. Аналоги соматостатина (октреотид, ланреотид).
Андрогены (см. Андрогены, антиандрогены) иногда применяют при метастатическом раке молочной железы. Назначают их женщинам с сохраненным менструальным циклом и в том случае, когда продолжительность менопаузы не превышает 5 лет. Нежелательными эффектами андрогенов, особенно при применении больших доз, являются вирилизация у женщин (огрубение голоса, чрезмерный рост волос на лице), задержка воды и солей в организме и др. Начало применения андрогенов (в частности тестостерона) для лечения рака молочной железы относят к 40-м гг. XX в.
Начиная с 1951 г. при лечении рака молочной железы широко используются прогестины (см. Эстрогены, гестагены; их гомологи и антагонисты). Гестагенные препараты применяют также для лечения рака эндометрия и рака почек, но мало используют для лечения рака простаты.
Основным показанием к назначению эстрогенов, начало использования которых в онкологической практике также относится к 40-м гг. XX в., является рак предстательной железы. При раке молочной железы их теперь назначают очень редко.
Важную роль в механизме действия гормональных препаратов играет их связывание со специфическими рецепторами, обнаруженными в тканях и некоторых опухолях.
Антиэстрогены конкурентно связываются с эстрогеновыми рецепторами в органах-мишенях и препятствуют образованию эстрогенрецепторного комплекса с эндогенным лигандом — 17-бета-эстрадиолом. В результате они тормозят стимулируемый эстрогенами рост опухоли. Чем больше эстрогенных рецепторов в опухоли — тем благоприятнее результат лечения антиэстрогенами.
Эффективным антиэстрогеном является тамоксифен — эталонный препарат для лечения рака молочной железы (особенно у женщин в менопаузе). Клиническое использование тамоксифена было начато в 1973 г. В настоящее время тамоксифен является широко используемым препаратом как для проведения адъювантной терапии, так и при лечении больных с диссеминированным процессом. Показано, что тамоксифен эффективен при всех стадиях заболевания, хорошо переносится при приеме в терапевтических дозах. Кроме основного показания — рак молочной железы у женщин — тамоксифен применяют при лечении рака грудной железы у мужчин, рака эндометрия, рака предстательной железы и др.
К антиандрогенам относят ряд соединений стероидной и нестероидной структур, способных подавлять физиологическую активность эндогенных андрогенов. Их действие связано с конкурентным блокированием рецепторов андрогенов в тканях-мишенях, биосинтез и секрецию андрогенов они не нарушают. Антиандрогенное действие свойственно в той или иной степени ряду эндогенных стероидных соединений, в т.ч. прогестинам, эстрогенам и их синтетическим производным, а также некоторым производным самих андрогенов. Из стероидных антиандрогенов наиболее известен ципротерон. В 70-х гг. XX в. появились сообщения о высокой антиандрогенной активности нестероидных соединений — производных карбоксианилида (флутамид и др.). Применяют антиандрогены в основном при раке предстательной железы. Область их использования включает также гиперандрогенные состояния у женщин (гирсутизм, облысение и др.), раннее половое созревание у детей.
Среди антиандрогенов выделяют вещества, которые только блокируют андрогенные рецепторы (т.н. чистые андрогены) — бикалутамид, флутамид, и вещества, которые, кроме способности блокировать рецепторы, имеют гонадотропную активность (т.н. антиандрогены двойного действия) — ципротерон.
Флутамид и бикалутамид блокируют связывание андрогенов с клеточными рецепторами, вследствие чего препятствуют проявлению биологических эффектов андрогенов в андрогенчувствительных органах, в т.ч. в клетках предстательной железы, и таким образом препятствуют росту опухоли. После приема флутамида отмечается повышение плазменных уровней тестостерона и эстрадиола.
Ципротерон обладает более выраженным андрогенным действием, т.к. помимо блокирования действия дигидротестостерона на уровне рецепторов, подавляет высвобождение гонадотропинов и, следовательно, синтез андрогенов. Одновременно с тестостероном в крови снижается содержание ЛГ и ФСГ.
Особым видом антиандрогенной активности обладают соединения, ингибирующие 5-альфа-редуктазу — внутриклеточный фермент предстательной железы, способствующий превращению тестостерона в более активный андроген — дигидротестостерон (ДГТ). Одним из ингибиторов 5-альфа-редуктазы является финастерид, применяющийся при лечении доброкачественной гиперплазии предстательной железы (см. Средства, влияющие на обмен веществ в предстательной железе, и корректоры уродинамики).
Гипоталамические рилизинг-факторы — эндогенные пептидные соединения, оказывающие влияние на высвобождение гипофизом гонадотропных гормонов (в т.ч. лютеинизирующего и фолликулостимулирующего). В настоящее время в медицинских целях используют не естественные рилизинг-факторы из гипоталамуса животных (овец, свиней), а их синтетические аналоги. Аналоги (как агонисты, так и антагонисты) полипептидных гормонов создают путем присоединения, выделения, замещения или изменения некоторых аминокислот в полипептидной цепочке природного гормона. Гонадотропин-рилизинг-гормон (ГнРГ) — гонадорелин, гонадолиберин, гонадотропин-рилизинг фактор — один из представителей класса рилизинг-гормонов гипоталамуса. ГнРГ в большей степени влияет на секрецию ЛГ, нежели ФСГ, поэтому часто его называют также рилизинг-гормоном лютеинизирующего гормона (ЛГРГ) .
ГнРГ представляет собой декапептид, состоящий из 10 аминокислот. Установлено, что аминокислоты в положении 2 и 3 ответственны за биологическую активность ГнРГ. Аминокислоты в положении 1, 6, 10 имеют структурную конфигурацию, необходимую для связывания с рецепторами клеток гипофиза. Замещение молекулы ГнРГ в положении 6 и 10 позволило создать агонисты рилизинг-гормона.
Синтетические гонадолиберины — нафарелин, гозерелин, гистрелин, лейпрорелин — аналоги гонадотропин-рилизинг-гормона — содержат D-аминокислоты в положении 6 и этиламидзамещающий глицин в положении 10. Результатом замены аминокислотных остатков в молекуле природного гормона является более выраженное сродство к рецепторам ГнРГ и более продолжительный период полураспада, поэтому аналоги имеют более сильное и более длительное действие, чем нативный гонадотропин-рилизинг-гормон. Так, активность гозерелина превышает активность нативного ГнРГ в 100 раз, трипторелина — в 36 раз, бусерелина — в 50 раз, а T1/2 синтетических гонадотропинов — 90–120 мин — намного превышает T1/2 нативного ГнРГ.
В мировой клинической практике известно более 12 лекарственных препаратов-аналогов ГнРГ: бусерелин, гистрелин, гозерелин, лейпрорелин, лутрелин, нафарелин, трипторелин, фертирелин и др. В России зарегистрированы лишь некоторые из них. Применяемые в России противоопухолевые средства — аналоги ГнРГ (гозерелин, лейпрорелин, трипторелин, бусерелин) сходны по структуре, механизму действия, основным фармакокинетическим и фармакодинамическим характеристикам, а также клинической эффективности и безопасности.
Гонадорелин секретируется гипоталамусом не постоянно, а в импульсном режиме, при этом пики следуют друг за другом с определенными интервалами, различными у мужчин и женщин: у женщин ГнРГ выделяется каждые 15 мин (фолликулярная фаза цикла) или 45 мин (лютеиновая фаза цикла и период беременности), у мужчин — 90 мин. ГнРГ обнаружен у всех млекопитающих. Пульсирующее выделение ГнРГ из гипоталамуса поддерживает выработку гонадотропинов в гипофизе.
Аналоги ГнРГ были предложены для клинического использования в 80-е гг. XX в. Эти лекарственные средства оказывают двухфазное действие на гипофиз: взаимодействуя с рецепторами ГнРГ клеток передней доли гипофиза, вызывают кратковременную стимуляцию с последующей длительной десенситизацией, т.е. снижением чувствительности рецепторов аденогипофиза к ГнРГ. После однократной инъекции аналога ГнРГ в результате стимулирующего эффекта усиливается секреция из передней доли гипофиза ЛГ и ФСГ (проявляется повышением содержания тестостерона в крови у мужчин и эстрогенов у женщин), обычно этот эффект наблюдается в первые 7–10 дней. При постоянном длительном применении аналоги гонадорелина подавляют высвобождение ЛГ и ФСГ, снижают функцию яичек и яичников и, соответственно, содержание половых гормонов в крови. Эффект проявляется примерно через 21–28 дней, при этом концентрация тестостерона в крови у мужчин снижается до уровня, наблюдаемого после хирургической кастрации (т.н. «лекарственная кастрация»), а уровень эстрогенов в крови у женщин — до уровня, наблюдаемого в постменопаузе. Эффект является обратимым и после окончания приема препаратов физиологическая секреция гормонов восстанавливается.
Применяют аналоги ГнРГ при раке предстательной железы — они способствуют регрессу опухоли простаты. Женщинам назначают при гормонозависимых опухолях молочной железы, эндометриозе, фиброме матки, т. к. они вызывают истончение эндометрия, уменьшение симптоматики и размеров объемных образований. Кроме того, аналоги ГнРГ применяют при лечении бесплодия (в программах экстракорпорального оплодотворения).
Побочные эффекты этих ЛС, возникающие в начале лечения и обусловленные временной стимуляцией гипофиза, проявляются в усилении симптомов, либо появлении дополнительных симптомов основного заболевания. Эти явления не требуют отмены препарата. Избежать их при лечении рака предстательной железы позволяет одновременное назначение на 2–4 неделе антиандрогена.
Наиболее часто встречающимися нежелательными эффектами у мужчин являются «приливы», снижение либидо, импотенция, гинекомастия. У женщин часто отмечаются «приливы», усиление потоотделения и изменение либидо. При применении аналогов ГнРГ у женщин существует риск усиления снижения плотности костных трабекул в позвонках (может быть необратимым). За период 6-месячного лечения это снижение плотности незначительно, за исключением больных с факторами риска (например остеопороз).
Аналоги ГнРГ выпускаются в различных лекарственных формах — для п/к, в/м, интраназального применения. Внутрь эти ЛС не назначаются, т.к. декапептиды легко расщепляются и инактивируются в ЖКТ. Учитывая необходимость длительного лечения, аналоги ГнРГ выпускаются также в виде лекформ пролонгированного действия, в т.ч. микрокапсул, микросфер.
Большая скорость разрушения ГнРГ (2–8 мин) не позволяет использовать его в клинической практике для длительного применения. Для ГнРГ величина T1/2 из крови составляет 4 мин, при п/к или интраназальном введении его аналогов — примерно 3 ч. Биотрансформация осуществляется в гипоталамусе и гипофизе. При почечной или печеночной недостаточности коррекции режима дозирования, как правило, не требуется.
Ингибиторы ароматазы начали применяться в онкологической практике в 70–80-е гг. XX в. Ароматаза — цитохром Р450-зависимый фермент, отвечающий за превращение синтезирующихся в коре надпочечников андрогенов в эстрогены. Ароматаза присутствует в различных тканях и органах, включая яичники, жировую ткань, скелетные мышцы, печень, а также ткань опухоли молочной железы. У женщин в пременопаузе основным источником циркулирующих эстрогенов являются яичники, тогда как в постменопаузе эстрогены образуются главным образом вне яичников. Ингибирование ароматазы приводит к уменьшению образования эстрогенов у женщин как в пременопаузе, так и в постменопаузе. Однако в пременопаузе снижение биосинтеза эстрогенов компенсируется усилением синтеза гонадотропинов по принципу обратной связи — снижение синтеза эстрогенов в яичниках стимулирует выработку гипофизом гонадотропинов, которые, в свою очередь, усиливают синтез андростендиона, и уровень эстрогенов вновь повышается. В связи с этим ингибиторы ароматазы неэффективны у женщин в пременопаузе. В постменопаузе, когда яичники перестают функционировать, ось гипоталамус — гипофиз — надпочечники разорвана, и ингибирование ароматазы приводит к значительному подавлению биосинтеза эстрогенов в периферических тканях, а также в ткани опухоли молочной железы.
Первым и фактически единственным представителем ингибиторов ароматазы I поколения является аминоглутетимид — неселективный ингибитор ароматазы. Поскольку аминоглутетимид ингибирует целый ряд ферментов, участвующих в стероидогенезе (подавляет секрецию надпочечниками глюкокортикоидов (кортизола) и используется поэтому при болезни Иценко — Кушинга и др.), при его применении необходимо следить за функциональным состоянием коры надпочечников (может развиться ее гипофункция).
Поиски новых средств, обладающих большей селективностью, лучшей переносимостью и более удобным режимом дозирования, привели к появлению ингибиторов ароматазы II и III поколений. К настоящему времени созданы новые нестероидные (летрозол, анастрозол и др.) и стероидные (эксеместан) соединения этой группы.
Основным показанием для ингибиторов ароматаз является рак молочной железы у женщин в постменопаузе, в т.ч. при резистентности к терапии антиэстрогенами.
К группе ингибиторов биосинтеза гормонов надпочечников, используемых в онкологии, относят митотан и аминоглутетимид. Они подавляют секрецию глюкокортикоидов и могут вызывать деструкцию нормальной и опухолевой ткани коры надпочечников.
Глюкокортикоиды — преднизолон, дексаметазон (см. Глюкокортикостероиды) в связи с их лимфолитическим действием и способностью угнетать митоз лимфоцитов применяют при острых лейкозах (главным образом у детей) и злокачественных лимфомах.
В качестве противоопухолевых средств применяют также некоторые аналоги соматостатина. Например, октреотид и ланреотид используют для симптоматической терапии эндокринных опухолей гастроэнтеропанкреатической системы.
Препараты
Препаратов —
2680; Торговых названий —
169; Действующих веществ —
37
Источник
Рак молочной железы относят к гормонозависимым опухолям, поэтому очень действенным считается проведение гормонотерапии при раке молочной железы.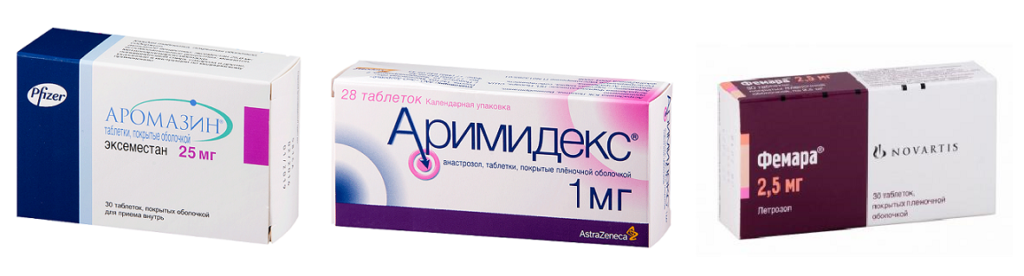
Что такое гормонотерапия и когда она применяется
Гормонотерапия это один из способов терапии онкологии молочной железы, среди которых химиотерапия, радиотерапия и хирургический способ лечения. Гормонотерапия преследует своей целью уменьшить воздействие гормона эстрогена на раковое новообразование.
Метод лечения гормонами составляет специалист, он учитывает стадию заболевания, статус менопаузы женщины, риск рецидивного возникновения раковой опухоли. Очень важно сочетать лечение онкологии груди с другими заболеваниями, так их присутствие может усилить побочные эффекты.
При лечении такого вида рака применяются различные виды лечения, в постменопаузе отличный результат выдают лекарственные препараты, которые понижают выработку гормона эстрогена, а в репродуктивном возрасте применяют релизинг-гормоны.
Назначение гормональной терапии показано, если биопсия показала, что рак является гормонозависимым и это делает лечение в 70% случаев успешным.
Ведущие клиники в Израиле
Гормонозависимая опухоль груди появляется, если повышается гормон эстроген, а его повышение возможно при использовании его при лечении:
- поликистоза яичников;
- нарушений месячных;
- миомы матки.
К группе риска можно отнести женщин, которые:
- имеют сбои в работе яичников;
- сделали аборт;
- имели угрозу выкидыша;
- перенесли замершую беременность.
Симптомами гормонозависимой опухоли груди считаются:
- увеличение лимфоузлов;
- боли в месте новообразований;
- появление уплотнений.
Показателями для рекомендации лечения гормонотерапией при гормонозависимых опухолях являются:
- наследственный фактор;
- внушительные размеры опухоли;
- рак на последней стадии;
- метастатический рак;
- для предотвращения рецидива после лечения карциномы;
- возникновение метастаз.
 Как правило, гормонотерапия назначается после хирургического вмешательства для подстраховки. Хирургическое удаление значительно уменьшает опасность возникновения рецидива онкологического заболевания молочной железы. Но абсолютной гарантии такое лечение, все же, не дает. Гормонотерапия гораздо эффективнее в лечении гормонозависимого рака груди, чем применение химиотерапии. Хотя в некоторых случаях эти две методики назначают одновременно. Их использование дает возможность блокировать эстрогеновые рецепторы и уничтожает их в крови. Конечно, в использовании этой методики есть свои плюсы и минусы.
Как правило, гормонотерапия назначается после хирургического вмешательства для подстраховки. Хирургическое удаление значительно уменьшает опасность возникновения рецидива онкологического заболевания молочной железы. Но абсолютной гарантии такое лечение, все же, не дает. Гормонотерапия гораздо эффективнее в лечении гормонозависимого рака груди, чем применение химиотерапии. Хотя в некоторых случаях эти две методики назначают одновременно. Их использование дает возможность блокировать эстрогеновые рецепторы и уничтожает их в крови. Конечно, в использовании этой методики есть свои плюсы и минусы.
Уменьшение уровня эстрогенов и прогестерона в крови проявляет, в общем, положительное воздействие на здоровье женщины, это снижает вероятность рецидива гормонозависимого заболевания.
Особенности использования гормонотерапии при раке груди
Гормонотерапию целесообразнее проводить в сочетании с прочими способами лечения. Назначение лечения гормональными препаратами проводят при:
- Вероятности появления метастазов;
- Различных уплотнениях после проведения операции;
- Раке, не поддающегося химиотерапии;
- Росте новообразования в отсутствии роста онкоклеток.
Запомните! Терапия рака молочной железы при помощи гормонотерапии разрешает одновременно несколько проблем, каждая из которых требует использование определенного препарата.
Выбор метода воздействия зависит от некоторых факторов:
- Предыдущих способов лечения;
- Гормонального статуса раковой опухоли;
- Стадии онкологического заболевания;
- Непереносимости препаратов;
- Сопутствующих диагнозов (некоторые болезни ухудшают прогнозы основного заболевания);
- Периода жизни пациента – пре- и постменопауза.
Так же при назначении лечения требуется знать, присутствуют ли в опухоли рецепторы к гормонам, и к которым именно. От гормонального статуса заболевания зависит и назначение лечения. Наиболее благоприятный прогноз, когда есть рецепторы одновременно к прогестерону и эстрогену, также бывают случаи:
- Негативности ко всем гормонам;
- Неизвестного гормонального статуса;
- Чувствительности только к эстрогену (прогестерону), когда рецептор эстрогена (прогестерона) позитивный.
Виды
Гормонотерапия рака молочной железы (РМЖ) подразделяется на три вида:
- Адъювантная гормонотерапия может длиться около 5-10 лет, она выполняется для уменьшения риска рецидива карциномы;
- Неоадъювантная гормонотерапия проводится в промежутке 3-6 месяцев, ее назначают перед операцией, когда опухоль более 2 см и в процесс втянуты лимфоузлы;
- Лечебная гормонотерапия применяется при неоперабельных опухолях или для уменьшения и устранения раковых очагов (больше 2 стадии (2а)).
Не тратьте время на бесполезный поиск неточной цены на лечение рака
* Только при условии получения данных о заболевании пациента, представитель клиники сможет рассчитать точную цену на лечение.
Какие препараты используются
 Гормональные препараты подбираются индивидуально и используются различными способами: отдельно, последовательно один за другим или в комбинации друг с другом. При обнаружении заболевания на последнем этапе, когда опухоль считается неоперабельной, гормонотерапия проводится для продления жизни пациентки.
Гормональные препараты подбираются индивидуально и используются различными способами: отдельно, последовательно один за другим или в комбинации друг с другом. При обнаружении заболевания на последнем этапе, когда опухоль считается неоперабельной, гормонотерапия проводится для продления жизни пациентки.
Можно выделить несколько ведущих видов гормонального лечения, любой из которых имеет отдельный механизм воздействия: понижение уровня эстрогена в крови, прекращение его выработки или ее уменьшение:
- Ингибиторы ароматазы. Они оказывают влияние на концентрацию эстрогенов, блокируя рецепторы и не давая клеткам размножаться и делиться. Такие ингибиторы прописываются больным после наступления менопаузы. Можно выделить 3 вида ингибиторов ароматазы при онкологии груди: Фемара, Аримидекс, Аромазин. Но эти препараты могут привести к повышению хрупкости костей. При приеме подобных препаратов назначается кальций с витамином D, для предотвращения остеопороза;
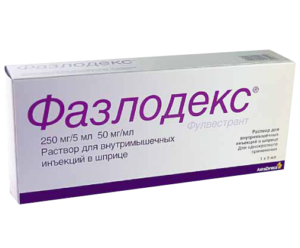
- Блокираторы эстрогеновых рецепторов, при эстрогенозависимых опухолях. Эти препараты предотвращают воздействие на клетки раковой опухоли. К таким препаратам можно отнести: Фулвестрант, Фазлодекс;
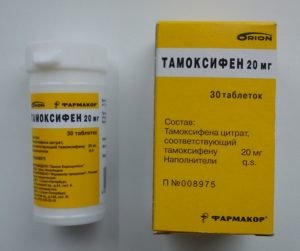
- Модуляторы рецепторов к эстрогенам, которые останавливают выработку эстрогенов. Это антиэстрогенные препараты в таблетках: Кломифен, Тамоксифен;
- Прогестины, которые уменьшают выработку определенных гормонов гипофиза, которые ответственны за появление андрогенов и эстрогенов;
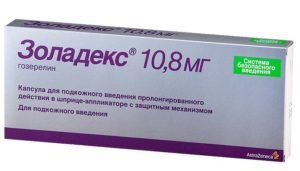
- Воздействие на яичники — еще один способ гормонотерапии. Таких способов три: медикаментозный (инъекции Золадексом или Люпроном), хирургический (удаление яичников — овариэктомия), радиационное облучение.
Читайте также: лечение онкологии в израиле
Последствия гормонотерапии
При лечении возможны побочные эффекты, появление которых зависит от множества факторов: стадии онкологического заболевания молочной железы, когда было получено лечение, возрастной категории пациентки, общего состояния здоровья, схемы назначенного лечения. Самыми частыми побочными эффектами являются:
- Преждевременный климакс и сопутствующие ему симптомы – приливы, увеличение веса и т.д.;
- Отечность ног;
- Проблемы со сном;
- Нарушение пищеварения (запоры или поносы);
- Боли в деснах;
- Сухость влагалища;
- Тошнота или рвота;
- Алопеция;
- Усиленная потливость;
- Депрессия;
- Ухудшение памяти.
В основном, эти симптомы через непродолжительное время проходят (спустя несколько недель по завершению лечения гормонами), иногда может продолжаться до 2 месяцев.
Ингибиторы ароматазы могут спровоцировать возникновения остеопороза, повышают холестерин в крови, могут вызвать проблемы с ЖКТ и приводят к алопеции.
Тамоксифен повышает риск тромбообразования, гепатита, является фактором риска для возникновения рака матки и проблем бесплодия.
 Фазлодекс способствует нарушениям деятельности мочевыделительной системы – цистит, а также вызывает расстройство стула и приступов аллергии на коже.
Фазлодекс способствует нарушениям деятельности мочевыделительной системы – цистит, а также вызывает расстройство стула и приступов аллергии на коже.
Золадекс и Люпрон вызывают скачки давления, артралгию, депрессию.
После хирургического удаления яичников может нарушаться водно-солевой обмен, может развиться алкалоз, поднятие уровня сахара в крови, также может диагностироваться синдром Кушинга и язвенные поражения органов ЖКТ.
При приеме прогестинов возможно прибавление веса, выпадение волос, тромбоэмболические осложнения.
Питание при использовании гормонотерапии
Диета при лечении гормонотерапией может понизить вероятность появления рецидива заболевания. В питании предпочтение надо отдавать отварным или тушеным блюдам, исключив полностью жареное. Также ограничения касаются употребления сахара, солений, жиров животного происхождения. Полностью исключить требуется:
- Консерванты;
- Кофе;
- Сою;
- Фастфуд;
- Продукты с пищевыми добавками;
- Алкоголь.
Из мясных блюд желательно употреблять нежирные сорта мяса, рекомендуется добавлять в пищу лук и чеснок. Пить побольше жидкости, простой воды. В рационе должны присутствовать следующие продукты:
- Морепродукты;
- Крупы;
- Фрукты;
- Растительные жиры;
- Жирная морская рыба;
- Морская капуста;
- Яйца;
- Овощи;
- Молочные продукты.
Эффективность гормонотерапии и прогноз при таком лечении
Эффективность гормонотерапии при онкологии молочной железы зависит от размера опухоли, также играет немаловажную роль наличие сопутствующих заболеваний и иммунитет пациентки.
Эффективность лечения гормонотерапией довольно высока, но требуется соблюдение всех рекомендаций врача, в том числе относительно питания.
Прогнозы гормонотерапии довольно оптимистичны, особенно, если гормонозависимая опухоль имеет рецепторы, и прогестерона, и эстрогена, тогда эффективность лечения составляет – 70 % случаев, при нахождении в опухоли, хотя бы одного из гормонов – эффективность составляет 30%. При прочих видах карциномы груди эффективность терапии составляет всего лишь 10%. При опухоли, которая считается негормонозависимой, такой тип лечения применять нецелесообразно.
Вопрос-ответ
Нужна ли гормонотерапия после мастэктомии?
Для предотвращения появления метастаз гормонотерапию могут назначить после хирургического вмешательства.
Источник


